题目内容
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500ml 2mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为
A.0.2mol B.0.6mol
C.0.8mol D.1.0mol
C
【解析】
试题分析:51.2g的Cu的物质的量是51.2g/64g/mol=0.8mol,则该过程中转移电子的物质的量是0.8mol×2=1.6mol,设NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为x,根据得失电子守恒,则整个过程中相当于+5价N元素得到电子生成+3价N元素,所以1.6mol=2x,则x=0.8mol,答案选C。
考点:考查氧化还原反应的计算

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列电池工作时,O2在正极放电的是
|
|
|
|
A.锌锰电池 | B.氢燃料电池 | C.铅蓄电池 | D.镍镉电池[ |
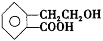 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。




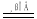 MnCl2+C12↑+2H2O.下列说法错误的是
MnCl2+C12↑+2H2O.下列说法错误的是