题目内容
12.对可逆反应2A(s)+3B(g)?C(g)+2D(g)△H<0,在一定条件下达到平衡,下列有关叙述正确的是( )①增加A的量,平衡向正反应方向移动
②升高温度,反应速率增大,平衡向逆反应方向移动
③压缩容器增大压强,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高.
| A. | ①② | B. | ② | C. | ①③ | D. | ②④ |
分析 ①A为纯固体,改变量,对平衡移动无影响;
②该反应为放热反应,升高温度,反应速率增大,向吸热方向移动;
③该反应为气体体积不变的反应,增大压强,正逆反应速率同等程度增大;
④增大反应物的浓度,平衡正向移动;
⑤催化剂对平衡移动无影响.
解答 解:①A为纯固体,增加A的量,平衡不移动,故错误;
②该反应为放热反应,升高温度,反应速率增大,向吸热方向移动,则平衡向逆反应方向移动,故正确;
③该反应为气体体积不变的反应,增大压强,正逆反应速率同等程度增大,平衡不移动,故错误;
④增大反应物的浓度,平衡正向移动,则v(正)>v(逆),故正确;
⑤催化剂对平衡移动无影响,则加入催化剂,B的转化率不变,故错误;
故选D.
点评 本题考查化学平衡的移动,为高频考点,把握温度、浓度、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意A为固体及反应的特点,题目难度不大.

练习册系列答案
相关题目
2.已知1mol白磷完全转化为红磷放出29.2kJ热量,下列两个反应:P4(白,s)+5O2(g)═2P2O5(s)△H=-Q1,4P(红,s)+5O2(g)═2P2O5(s)△H=-Q2,Q1与Q2的关系是( )
| A. | Q1=Q2 | B. | Q1>Q2 | C. | Q1<Q2 | D. | 无法确定 |
3.将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述中不正确的是( )
| A. | 表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠 | |
| B. | “出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液 | |
| C. | “出汗”→变成白色固体(粉末)过程中只发生物理变化 | |
| D. | 最后变成碳酸钠粉末 |
20.下列说法中正确的是( )
| A. | 任何一个水分子,其本身都是固体 | |
| B. | 逐渐加热升温,碳酸氢铵也可体现出三态变化 | |
| C. | 面包是固体,但在受压时体积缩小,故可以说固体易被压缩 | |
| D. | 在水蒸气、液态水和冰中,水分子都在不停地运动 |
7.下列物质中所含分子物质的量最多的是( )
| A. | 88g CO2 | B. | 3 mol H2 | ||
| C. | 128 g SO2 | D. | 6.02×1023个硫酸分子 |
17.在盛放浓硫酸的试剂瓶标签上应该印有下列警示标记中的( )
| A. |  爆炸品 | B. |  易燃液体 | C. |  剧毒品 | D. |  腐蚀品 |
4.化学与生产、生活、社会密切相关,下列说法正确的是( )
| A. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 小苏打是制作面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 浓硫酸可刻蚀石英制艺术品 | |
| D. | 煤经过气化和液化等物理变化可以转化为清洁燃料 |
1.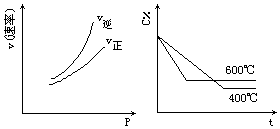 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )| A. | N2O3(g)?NO2(g)+NO(g)-Q | B. | 3NO2(g)+H2O(l)?2HNO3 (aq)+NO(g)+Q | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+Q | D. | CO2(g)+C(s)?2CO(g)-Q |