题目内容
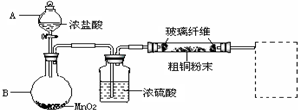
6.已知A为单质,与某物质反应生成气体与B.有以下物质相互转化;
试回答:
(1)写出B的化学式FeCl2;D的化学式KCl;
(2)写出由D转变成H的化学方程式Cl-+Ag+═AgCl↓;
(3)写出由F转变成G的离子方程式4Fe(OH)2+2H2O+O2=4Fe(OH)3.
分析 白色沉淀E在空气中转化为红褐色沉淀F,则E为Fe(OH)2,F为Fe(OH)3,F与盐酸反应得到G,G与单质A反应得到B,结合转化关系及元素守恒可知,A为Fe,G为FeCl3,B为FeCl2,B与C溶液反应得到D,D与AgNO3生成白色沉淀H,可知H为AgCl,透过蓝色钴玻璃观察焰色反应为紫色,可知D溶液中含有K+,故D为KCl,C为KOH,金属单质A与稀盐酸反应会生成B溶液和放出气体H2,然后结合物质的性质及化学用语来解答.
解答 解:(1)由上述分析可知,B为FeCl2,D为KCl,故答案为:FeCl2;KCl;
(2)由D转变成H的离子方程式为:Cl-+Ag+═AgCl↓,故答案为:Cl-+Ag+═AgCl↓;
(3)Fe(OH)2在空气中与O2反应转变为Fe(OH)3,反应为4Fe(OH)2+2H2O+O2=4Fe(OH)3,
故答案:4Fe(OH)2+2H2O+O2=4Fe(OH)3.
点评 本题考查无机物的推断,E到F的颜色变化及焰色反应等时推断突破口,侧重铁及其化合物的性质及转化的考查,题目难度不大.

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
16.将 4molA气体和 2molB气体在 2L 固定体积的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g).若经2s后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质 A 表示的反应的平均速率为 0.3 mol•L-1•s-1 | |
| B. | 用物质 B 表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质 A 的转化率为70% | |
| D. | 2 s 时物质 B 的浓度为 0.7 mol•L-1 |
17.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | H2 | B. | CH4 | C. | HCl | D. | Cl2 |
14.为了证明醋酸是弱电解质,四同学分别进行实验:
甲用pH试纸测出0.10mol/L的醋酸溶液pH=4;
乙将pH=3醋酸和盐酸,各取10ml,用蒸馏水稀释到原来的100倍,然后用pH试纸测定该溶液的pH,醋酸的变化小
丙将pH=3醋酸和盐酸,分别加入相应的钠盐固体,醋酸的pH变化大
丁取pH=3的盐酸和醋酸,分别稀释到原来的100倍,然后加入完全一样的锌粒,测量醋酸放出H2的速率快
上述实验可以实现并能证明醋酸是弱酸的是( )
甲用pH试纸测出0.10mol/L的醋酸溶液pH=4;
乙将pH=3醋酸和盐酸,各取10ml,用蒸馏水稀释到原来的100倍,然后用pH试纸测定该溶液的pH,醋酸的变化小
丙将pH=3醋酸和盐酸,分别加入相应的钠盐固体,醋酸的pH变化大
丁取pH=3的盐酸和醋酸,分别稀释到原来的100倍,然后加入完全一样的锌粒,测量醋酸放出H2的速率快
上述实验可以实现并能证明醋酸是弱酸的是( )
| A. | 一位同学 | B. | 二位同学 | C. | 三位同学 | D. | 四位同学 |
11.下列说法正确的是( )
| A. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| B. | 焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 | |
| C. | 钢铁发生电化学腐蚀时,负极的电极反应式为 Fe-3e-=Fe3+ | |
| D. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
18.化学与生产、生活密切相关,下列说不正确的是( )
| A. | 合成纤维和光导纤维都属于新型无机非金属材料 | |
| B. | “地沟油”禁止食用,但经过加T处理后,可以用来制取肥皂和生物柴油 | |
| C. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| D. | 利用丁达尔效应鉴别 Fe(OH)3胶体和FeCl3溶液 |