题目内容
铜及其化合物在生产、生活中有广泛的应用.
(1)铜可采用如下方法制备:火法炼铜:Cu2S+O2
2Cu+SO2 湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被 (填“氧化”还是“还原”)成铜单质.
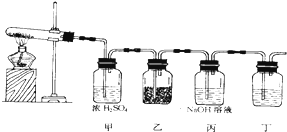
(2)印刷电路板上使用的铜需要回收利用.用FeCl3溶液浸泡印刷电路板制备CuCl2?2H2O,实验室模拟回收过程如图:

①步骤1中反应的离子方程式是 .
②步骤2所加的氧化剂最适宜的是 .
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到5,此时Fe3+浓度为 .[Ksp(Fe(OH)3)=4×10-38],可选用的“试剂1”是 (写出一种即可).
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是 (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2?2H2O.
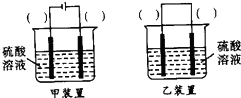
(3)欲实现反应Cu+H2SO4(aq)═CuSO4+H2↑,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”).并写出电极反应式.
(1)铜可采用如下方法制备:火法炼铜:Cu2S+O2
| ||
上述两种方法中,铜元素均被
(2)印刷电路板上使用的铜需要回收利用.用FeCl3溶液浸泡印刷电路板制备CuCl2?2H2O,实验室模拟回收过程如图:

①步骤1中反应的离子方程式是
②步骤2所加的氧化剂最适宜的是
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到5,此时Fe3+浓度为
④蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是
(3)欲实现反应Cu+H2SO4(aq)═CuSO4+H2↑,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”).并写出电极反应式.

考点:金属冶炼的一般原理,原电池和电解池的工作原理,物质分离和提纯的方法和基本操作综合应用
专题:电化学专题,元素及其化合物
分析:(1)反应物中元素的化合价降低,为氧化剂,被还原,发生还原反应;
(2)①根据步骤1中反应Cu+2FeCl3=2FeCl2+CuCl2书写离子方程式;
②根据根据除去二价铁离子的过程中不能引入新的杂质;
③根据溶液的pH升高到5时,H+浓度为 10-5mol/L,则OH-浓度为 10-9mol/L,根据Ksp(Fe(OH)3)=[Fe3+][OH-]3=4×10-38,得[Fe3+]=4×10-11mol/L;步骤3可选用的“试剂1”是既要能与酸反应,降低氢离子浓度,使溶液的pH升高,从而使Fe3+转化为Fe(OH)3沉淀而除去,又不引入新的杂质;
④CuCl2在溶液中可以发生水解反应,加入浓盐酸,可以抑制水解;
(3)Cu和H2SO4之间的反应是非自发的,需要电解池实现,根据电解池的构成条件来回答.
(2)①根据步骤1中反应Cu+2FeCl3=2FeCl2+CuCl2书写离子方程式;
②根据根据除去二价铁离子的过程中不能引入新的杂质;
③根据溶液的pH升高到5时,H+浓度为 10-5mol/L,则OH-浓度为 10-9mol/L,根据Ksp(Fe(OH)3)=[Fe3+][OH-]3=4×10-38,得[Fe3+]=4×10-11mol/L;步骤3可选用的“试剂1”是既要能与酸反应,降低氢离子浓度,使溶液的pH升高,从而使Fe3+转化为Fe(OH)3沉淀而除去,又不引入新的杂质;
④CuCl2在溶液中可以发生水解反应,加入浓盐酸,可以抑制水解;
(3)Cu和H2SO4之间的反应是非自发的,需要电解池实现,根据电解池的构成条件来回答.
解答:
解:(1)在火法炼铜:Cu2S+O2
2Cu+SO2和湿法炼铜:CuSO4+Fe═FeSO4+Cu中铜元素的化合价降低,Cu2S、CuSO4都为氧化剂,被还原,发生还原反应,
故答案为:还原;
(2)①步骤1中Cu元素由0升高到+2价,Fe元素由+3价降低为+2价,化学反应为Cu+2FeCl3═2CuCl2+FeCl2,离子反应为Cu+2Fe3+═2Cu2++Fe2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
②HNO3、H2O2C、KMnO4三者都能氧化二价铁离子变成三价铁离子,但HNO3和KMnO4会引入新的杂质,
故答案为:B;
③根据溶液的pH升高到5时,H+浓度为 10-5mol/L,则OH-浓度为 10-9mol/L,根据Ksp(Fe(OH)3)=[Fe3+][OH-]3=4×10-38,得[Fe3+]=4×10-11mol/L;
pH升高,溶液的酸性减弱,加入的物质能与酸反应,同时不能引入新杂质,可向溶液中加入CuO或Cu(OH)2,
故答案为:4×10-11 mol/L;CuO[或Cu(OH)2];
④CuCl2为强酸弱碱盐水解溶液呈酸性,溶液中水解反应为,CuCl2+2H2O?Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解;
故答案为:CuCl2在溶液中可以发生水解反应:CuCl2+2H2O?Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解;
(3)Cu和H2SO4之间的反应是非自发的,需要电解池实现,金属铜作阳极,阳极:Cu-2e-=Cu2+,电解质为硫酸,阴极是氢离子放电,电极反应为2H++2e-=H2↑,即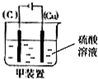 ,故答案为:
,故答案为: .
.
| ||
故答案为:还原;
(2)①步骤1中Cu元素由0升高到+2价,Fe元素由+3价降低为+2价,化学反应为Cu+2FeCl3═2CuCl2+FeCl2,离子反应为Cu+2Fe3+═2Cu2++Fe2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
②HNO3、H2O2C、KMnO4三者都能氧化二价铁离子变成三价铁离子,但HNO3和KMnO4会引入新的杂质,
故答案为:B;
③根据溶液的pH升高到5时,H+浓度为 10-5mol/L,则OH-浓度为 10-9mol/L,根据Ksp(Fe(OH)3)=[Fe3+][OH-]3=4×10-38,得[Fe3+]=4×10-11mol/L;
pH升高,溶液的酸性减弱,加入的物质能与酸反应,同时不能引入新杂质,可向溶液中加入CuO或Cu(OH)2,
故答案为:4×10-11 mol/L;CuO[或Cu(OH)2];
④CuCl2为强酸弱碱盐水解溶液呈酸性,溶液中水解反应为,CuCl2+2H2O?Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解;
故答案为:CuCl2在溶液中可以发生水解反应:CuCl2+2H2O?Cu(OH)2+2HCl,滴加浓盐酸,可以抑制水解;
(3)Cu和H2SO4之间的反应是非自发的,需要电解池实现,金属铜作阳极,阳极:Cu-2e-=Cu2+,电解质为硫酸,阴极是氢离子放电,电极反应为2H++2e-=H2↑,即
 ,故答案为:
,故答案为: .
.
点评:本题考查金属的回收,涉及到氧化还原反应、电解池的工作原理等知识,题目难度中等,注意电解池的工作原理是高频考点.

练习册系列答案
相关题目
下列各烃分别与H2完全加成,不能生成2,2,3-三甲基戊烷的是( )
A、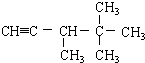 |
B、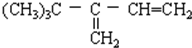 |
| C、CH2=CHC(CH3)2CH(CH3)2 |
D、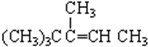 |
下列说法不正确的是( )
| A、1 mol氧气的质量为32 g |
| B、标准状况下,0.5 molNO和0.5 mol O2的混合后体积约为22.4 L |
| C、CO2的摩尔质量为44 g/mol |
| D、1 L 2 mol?L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |
下列表中对于相关物质的分类全部正确的一组是( )
| 编号 | 纯净物 | 混合物 | 弱电解质 | 非电解质 |
| A | 明矾 | 蔗糖 | NaHCO3 | CO2 |
| B | 天然橡胶 | 石膏 | NH3?H2O | CH3CH2OH |
| C | 冰 | 王水 | H2SiO3 | Cl2 |
| D | 胆矾 | 水玻璃 | H2CO3 | SO2 |
| A、A | B、B | C、C | D、D |
下列关于维生素的叙述中不正确的是( )
| A、根据维生素的溶解性可以将维生素分为脂溶性和水溶性两大类 |
| B、人体所需要的维生素都可以自身合成 |
| C、维生素C具有较强的还原能力,容易被氧化 |
| D、维生素的作用是维持细胞的正常功能、调节人体新陈代谢 |