题目内容
5.将下列有机化合物用系统命名法命名或根据名称写出其结构简式.(1)
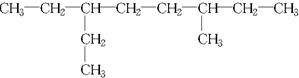
命名:3-甲基-6-乙基辛烷
(2)
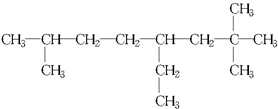
命名:2,2,7-三甲基-4-乙基辛烷
(3)2,6,6三甲基5乙基癸烷,结构简式:
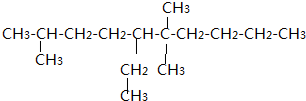 .
.(4)3,3二乙基戊烷:
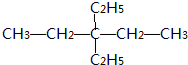 .
.
分析 烷烃的命名原则:碳链最长称某烷,靠近支链把号编,简单在前同相并,其间应划一短线:
1、碳链最长称某烷:选定分子里最长的碳链做主链,并按主链上碳原子数目称为“某烷“;
2、靠近支链把号编:把主链里离支链较近的一端作为起点,用1、2、3…等数字给主链的各碳原子编号定位以确定支链的位置;
3、简单在前同相并,其间应划一短线:把支链作为取代基,把取代基的名称写在烷烃名称的前面,在取代基的前面用阿拉伯数字注明它在烷烃主链上的位置,而且简单的取代基要写在复杂的取代基前面,如果有相同的取代基,则要合并起来用二、三等数字表示,但是表示相同的取代基位置的阿拉伯数字要用逗号隔开,并在号数后面连一短线,中间用“-“隔开.
解答 解:(1)最长碳链含有8个C,为辛烷,3号C上一个甲基,6号C上一个乙基,系统法命名为3-甲基-6-乙基辛烷,
故答案为:3-甲基-6-乙基辛烷;
(2)最长碳链含有8个C,为辛烷,2号C上两个甲基,7号C上一个甲基,4号C上一个乙基,系统法命名为2,2,7-三甲基-4-乙基辛烷,
故答案为:2,2,7-三甲基-4-乙基辛烷;
(3)写出10个C的碳链,从一端依次编号1-10,在2号C上连接一个甲基,6号C上连接两个甲基,5号C上连接一个乙基,最后补齐H,得到结构简式为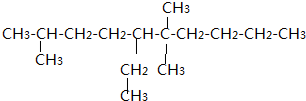
故答案为: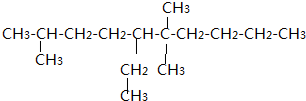 ;
;
(4)写出5个C的碳链,从一端依次编号1-5,在3号C上连接两个乙基,最后补齐H,得到结构简式为 ,
,
故答案为: .
.
点评 本题考查了有机物的命名,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,解题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可.

练习册系列答案
相关题目
15.某化学研究性学习小组拟测定食醋的总酸量(g/10mL),请你参与该小组的实验并回答相关问题.
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500mL(商标注明总酸量:3,.50g/100mL~5.00g/100mL),0.1000mol/L NaOH标准溶液;100mL容量瓶,10mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙,酚酞,石蕊).
[实验步骤]
①配制并移取待测食醋溶液
用10mL移液管吸取10mL市售白醋样品置于100mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20mL,并移至锥形瓶中.
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下.静置,读取数据并记录为NaOH标准溶液体积的初读数.
③滴定
往盛有待测食醋溶液的锥形瓶中的滴加某酸碱指示计2~3滴,滴定至终点.记录NaOH的终读数.重复滴定3次.
[数据记录]
[问题与思考]
(1)步骤①中用煮沸并迅速冷却的方法处理蒸馏水的目的是除去CO2,防止其对实验结果的影响.
(2)步骤③中你选择的酸碱指示剂是酚酞,理由是CH3COONa溶液呈碱性,应选择变色范围在碱性的指示剂.
(3)样品总酸量=4.50g/100mL.
(4)导致实验结果偏大的主要原因是①②(填写序号)
①滴定终点时,仰视滴定管读数
②滴定后滴定管尖嘴处悬有一滴液体
③移液管用蒸馏水洗净后,就用来吸取待测液
④滴定前,碱式滴定管无气泡,滴定后产生气泡
⑤锥形瓶只用蒸馏水洗涤后仍留有少量蒸馏水.
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500mL(商标注明总酸量:3,.50g/100mL~5.00g/100mL),0.1000mol/L NaOH标准溶液;100mL容量瓶,10mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙,酚酞,石蕊).
[实验步骤]
①配制并移取待测食醋溶液
用10mL移液管吸取10mL市售白醋样品置于100mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20mL,并移至锥形瓶中.
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下.静置,读取数据并记录为NaOH标准溶液体积的初读数.
③滴定
往盛有待测食醋溶液的锥形瓶中的滴加某酸碱指示计2~3滴,滴定至终点.记录NaOH的终读数.重复滴定3次.
[数据记录]
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(样品)/ml | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)始/ml | 0.00 | 0.20 | 0.10 | 0.10 |
| V(NaOH)终/ml | 14.98 | 15.20 | 15.12 | 16.24 |
(1)步骤①中用煮沸并迅速冷却的方法处理蒸馏水的目的是除去CO2,防止其对实验结果的影响.
(2)步骤③中你选择的酸碱指示剂是酚酞,理由是CH3COONa溶液呈碱性,应选择变色范围在碱性的指示剂.
(3)样品总酸量=4.50g/100mL.
(4)导致实验结果偏大的主要原因是①②(填写序号)
①滴定终点时,仰视滴定管读数
②滴定后滴定管尖嘴处悬有一滴液体
③移液管用蒸馏水洗净后,就用来吸取待测液
④滴定前,碱式滴定管无气泡,滴定后产生气泡
⑤锥形瓶只用蒸馏水洗涤后仍留有少量蒸馏水.
13.工业上制取金刚砂的化学方程式如下:SiO2+3C=SiC+2CO↑.在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )
| A. | 1:2 | B. | 2:1 | C. | 5:3 | D. | 3:5 |
20.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6.下列说法正确的是( )
| A. | Y元素最高价氧化物对应的水化物化学式H2YO4 | |
| B. | 原子半径由大到小的顺序为:Z>Y>W | |
| C. | X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 | |
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
17.下列关于烃性质的说法中正确的是( )
| A. | 乙烯可以与酸性高锰酸钾溶液反应,因此可以用酸性高锰酸钾溶液除去乙烷中混有的乙烯 | |
| B. | 溴乙烷可以通过乙烯与溴化氢加成得到,也可以通过乙烷与溴发生取代反应制备 | |
| C. | 区分甲苯和苯可以使用酸性高锰酸钾溶液,也可以用溴水 | |
| D. | 鉴别己烯中是否混有少量甲苯,正确的实验方法是可以加足量溴水,然后再加入酸性高锰酸钾溶液 |
14.下列说法正确的是( )
| A. | 通常状况下,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ•mol-1 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ•mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1 |
 在1.5L的密闭容器中通入2molX2和3molY2的混合气体,在一定条件下发生反应:X2(g)+3Y2(g)?2Z(g)+4W(?)△H<0达到平衡时,容器内压强为反应开始时的0.8(相同温度下测量).
在1.5L的密闭容器中通入2molX2和3molY2的混合气体,在一定条件下发生反应:X2(g)+3Y2(g)?2Z(g)+4W(?)△H<0达到平衡时,容器内压强为反应开始时的0.8(相同温度下测量).