题目内容
12.下列叙述正确的是( )| A. | 用NaOH溶液、蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+ | |
| B. | 用干燥的pH试纸可测得新制氯水的pH=2 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH-COOCH3 | |
| D. | 食盐中的碘可以直接用淀粉检验其是否存在 |
分析 A.红色石蕊试纸可检验氨气;
B.氯水中含HClO,具有漂白性;
C.有机物A(C4H6O2)能发生加聚反应,一定含碳碳双键;
D.食盐中的碘为碘酸钾,而淀粉遇碘单质变蓝.
解答 解:A.红色石蕊试纸可检验氨气,用NaOH溶液、蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+,故A正确;
B.氯水中含HClO,具有漂白性,不能用pH试纸测pH,应选pH计,故B错误;
C.有机物A(C4H6O2)能发生加聚反应,一定含碳碳双键,有机物为CH2=CH-COOCH3或CH2=CHCH2COOH、CH3CH=CHCOOH,故C错误;
D.食盐中的碘为碘酸钾,而淀粉遇碘单质变蓝,则直接用淀粉不能检验,故D错误;
故选A.
点评 本题考查有机物的结构、物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意选项C中有机物可能为烯酸,题目难度不大.

练习册系列答案
相关题目
2.在解释物质性质变化规律与物质结构间的因果关系时,与键能无关的变化规律是( )
| A. | Li、Na、K、Rb的沸点逐渐降低 | |
| B. | 与硅相比,金刚石的硬度大、熔点高 | |
| C. | HF、HCl、HBr、HI热稳定性依次减弱 | |
| D. | H2、O2、H2S在水中的溶解性依次为难溶、微溶、可溶 |
20.某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+7种离子中的几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气体冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:
该溶液中肯定不存在的离子是( )
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气体冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:
该溶液中肯定不存在的离子是( )
| A. | Al3+、Na+、SON32-、I- | B. | Mg2+、Na+、CO32-、Br- | ||
| C. | Al3+、Mg2+、I-、SO32- | D. | Al3+、CO32-、Br-、SO32- |
7.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
17.某基态原子的3d能级中有一个电子,其第四电子层中的电子数为( )
| A. | 0 | B. | 2 | C. | 3 | D. | 8 |
4.下列电子式中错误的是( )
| A. | Na+ | B. | 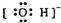 | C. | 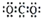 | D. | 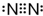 |
1.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下.

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、A13+、Ca2+和Mg2+.
(1)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(2)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.滤液II中阳离子主要有Na+、Mg2+、Ca2+;
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液II中的金属阳离子是Ca2+、Mg2+.
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、A13+、Ca2+和Mg2+.
(1)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(2)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | - | - | - |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液II中的金属阳离子是Ca2+、Mg2+.
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.