题目内容
20.下列表示中不正确的是( )| A. | 1 mol氧 | B. | 1 mol H | C. | 1 mol CO32- | D. | 1 mol NaCl |
分析 在用物质的量描述物质时,应指代明确,且摩尔后面应用化学式,而不能用名称,据此分析.
解答 解:在用物质的量描述微粒的集合体时,应指代明确,且摩尔后面应用化学式,而不能用名称,故A中1mol氧,指代不明,没指明是1molO还是1molO2,故A错误,BCD均正确.
故选A.
点评 本题考查了用物质的量的单位mol来描述物质,难度不大,应注意基础的掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.有5瓶白色固体试剂,分别是Ba(NO3)2、KCl、NaOH、CuSO4、和Na2SO4,现只提供蒸馏水,通过下面的实验步骤可鉴别它们.请填写下列空白.
(1)各取少量固体试剂加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是溶液呈蓝色.被检出的物质的化学式是CuSO4
(2)分别向剩下的4种溶液的试管中加入(1)中已检出的溶液,观察到的现象和相应的化学反应方程式是:
(3)最后可利用Ba(NO3)2的试剂(填化学式)鉴别余下未检出的物质.
(1)各取少量固体试剂加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是溶液呈蓝色.被检出的物质的化学式是CuSO4
(2)分别向剩下的4种溶液的试管中加入(1)中已检出的溶液,观察到的现象和相应的化学反应方程式是:
| 现象 | 化学反应方程式 | |
| ① | 试管中有白色沉淀生成 | Ba(NO3)2+CuSO4═BaSO4↓+Cu(NO3)2 |
| ② | 试管中有蓝色沉淀生成 | CuSO4+2NaOH═Cu(OH2)↓+2NaNO3 |
8.在主族元素中,X元素位于第二周期,且分别与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20.下列判断正确的是( )
| A. | 原子序数:Z<Y<X<W | |
| B. | X、Y、Z、W形成的单质最多有6种 | |
| C. | X元素最高价氧化物对应水化物的化学式为:HXO3 | |
| D. | 四种元素的气态氢化物中,W的气态氢化物最稳定 |
15.检验久置的FeSO4是否变质,最好选用的试剂是( )
| A. | 铁片 | B. | NaOH溶液 | C. | 石蕊溶液 | D. | KSCN溶液 |
5.下列反应的离子方程式书写中,正确的是( )
| A. | 金属钾溶于水:2K+2H2O═2K++OH-+H2↑ | |
| B. | 小苏打溶液中加入少量NaOH溶液:H++OH-═H2O | |
| C. | FeCl3溶液与铜反应:Fe3++Cu═Fe2++Cu2+ | |
| D. | 硫酸溶液中加入氢氧化钡溶液至中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
12.实验室用下图所示装置制备氯气并进行一系列相关的实验(夹持设备已省略).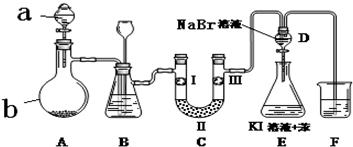
(1)a、b两仪器的名称:a分液漏斗;b蒸馏烧瓶.
(2)洗气装置B是为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)制备氯气选用的药品为:漂粉精固体【主要成分为Ca(ClO)2】和浓盐酸,相关的化学反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为黄色,说明氯的非金属性大于溴(填“大于”或“小于”).
(6)F处为烧碱溶液,写出吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.

(1)a、b两仪器的名称:a分液漏斗;b蒸馏烧瓶.
(2)洗气装置B是为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)制备氯气选用的药品为:漂粉精固体【主要成分为Ca(ClO)2】和浓盐酸,相关的化学反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 无水氯化钙 | 浓硫酸 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(6)F处为烧碱溶液,写出吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
10.钛元素被称为“崛起的第三金属”,已知钛有48Ti、49Ti、50Ti等核素,下列关于金属钛的叙述中不正确的是( )
| A. | 上述钛原子中,中子数不可能为22 | |
| B. | 钛元素位于元素周期表的d区,属过渡元素 | |
| C. | 钛原子的外围电子层排布为3d24s2 | |
| D. | 钛元素在周期表中处于第四周期ⅥB族 |

 ;
;
 .
.