题目内容
16.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | PH=1的稀硫酸中含有的H+数为0.1NA | |
| B. | 1mol苯分子中含有的碳碳双键数为3NA | |
| C. | 18gH2O中含有的质子数为10NA | |
| D. | 50mL12mol•L-1的盐酸与足量的MnO2共热,生成的Cl2分子数为0.15NA |
分析 A、溶液体积不明确;
B、苯不是单双键交替的结构;
C、求出水的物质的量,然后根据水中含10个质子来分析;
D、二氧化锰只能与浓盐酸反应,与稀盐酸不反应.
解答 解:A、溶液体积不明确,故溶液中的氢离子的个数无法计算,故A错误;
B、苯不是单双键交替的结构,故苯中无碳碳双键,故B错误;
C、18g水的物质的量为1mol,而水中含10个质子,故1mol水中含10mol质子即10NA个,故C正确;
D、二氧化锰只能与浓盐酸反应,与稀盐酸不反应,故浓盐酸不能反应完全,则生成的氯气分子个数小于0.15NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
6.出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面.下列说法不正确的是( )
| A. | 将金属制成合金,可以保持甚至强化单一金属的长处,克服其不足 | |
| B. | 在自然环境中,锡青铜中的锡对铜起保护作用 | |
| C. | 锡青铜文物在潮湿环境中的腐蚀比干燥环境中快 | |
| D. | 生成Cu2(OH)3Cl覆盖物是化学反应过程,但不是电化学腐蚀过程 |
7.实验室保存下列物质的方法中,不正确的是( )
| A. | HF溶液保存在玻璃试剂瓶中 | |
| B. | 液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封 | |
| C. | 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 硝酸应装在棕色瓶中密封避光保存 |
11.铬及其化合物在工业上有许多用途,但化工废料铬渣对人体健康有很大危害.
以制革工业产生的污泥为原料,回收污泥中三价铬的工艺流程如图所示,(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+):
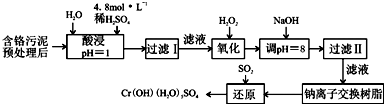
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)能提高酸浸时三价铬的浸取率的措施有ABC(填字母)
A.将含铬污泥粉碎并适当延长浸取时间 B.升高温度不断搅拌 C.多次浸取,合并浸取液 D.缩短浸取时间
(2)氧化过程中加入H2O2,除了能把Cr3+氧化为Cr2O72-外,另一个作用是2Fe2++2H++H2O2=2Fe3++2H2O(用离子方程式表示)
(3)过滤Ⅱ产生的沉淀是Fe(OH)3、Al(OH)3、Cu(OH)2,(填化学式)
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+,Mg2+(填离子符号)
(5)每生成1molCr(OH)(H2O)3SO4,消耗SO2的物质的量为1.5mol
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解,经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去
①铁电极与直流电源的正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)3]=6.0×10-31)
以制革工业产生的污泥为原料,回收污泥中三价铬的工艺流程如图所示,(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
A.将含铬污泥粉碎并适当延长浸取时间 B.升高温度不断搅拌 C.多次浸取,合并浸取液 D.缩短浸取时间
(2)氧化过程中加入H2O2,除了能把Cr3+氧化为Cr2O72-外,另一个作用是2Fe2++2H++H2O2=2Fe3++2H2O(用离子方程式表示)
(3)过滤Ⅱ产生的沉淀是Fe(OH)3、Al(OH)3、Cu(OH)2,(填化学式)
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+,Mg2+(填离子符号)
(5)每生成1molCr(OH)(H2O)3SO4,消耗SO2的物质的量为1.5mol
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解,经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去
①铁电极与直流电源的正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)3]=6.0×10-31)
8.下列关于有机物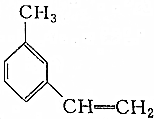 的命名正确的是( )
的命名正确的是( )
 的命名正确的是( )
的命名正确的是( )| A. | 1-甲基-3-乙基苯 | B. | 1-甲基-3-苯乙烯 | C. | 间甲基苯乙烯 | D. | 间乙基甲苯 |
2.如图1表示mA(g)+nB(g)?pC(g)+qD(g),在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;如图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的一个条件重新建立新平衡的反应过程,判断该反应是( )


| A. | m+n<p+q△H>0 | B. | m+n>p+q△H>0 | C. | m+n<p+q△H<0 | D. | m+n>p+q△H<0 |
3.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺如下(部分操作和条件略):
Ⅰ.将铬铁矿和碳酸钠混合充分焙烧.
Ⅱ.焙烧后的固体加水浸取,分离得到溶液A和固体A.
Ⅲ.向溶液A中加入醋酸调pH约7~8,分离得到溶液B和固体B.
Ⅳ.再向溶液B中继续加醋酸酸化,使溶液pH小于5.
Ⅴ.向上述溶液中加入氯化钾,得到重铬酸钾晶体.
(1)Ⅰ中焙烧发生的反应如下,配平并填写空缺:
①4FeO•Cr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2↑
②Na2CO3+Al2O3═2NaAlO2+CO2↑
(2)固体A中主要含有Fe2O3、MgO(填写化学式).
(3)已知重铬酸钾溶液中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O.Ⅳ中调节溶液pH<5时,其目的是由于存在反应平衡Cr2O72-+H2O?2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72-..
(4)Ⅴ中发生反应的化学方程式是:Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl
表是相关物质的溶解度数据:
①该反应能发生的理由是温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,低温下四种物质中K2Cr2O7的溶解度最小,利用复分解反应在低温下可以得到重铬酸钾.
②获得K2Cr2O7晶体的操作有多步组成,依次是:加入KCl固体、加热浓缩、冷却结晶、过滤、洗涤、干燥得到晶体.
(5)Ⅲ中固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析固体B中氢氧化铝含量的方法是:称取n g样品,加入过量氢氧化钠溶液(填写试剂名称)、溶解、过滤、再通入过量的CO2、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26m}{17n}$(用含m、n的代数式表示).
Ⅰ.将铬铁矿和碳酸钠混合充分焙烧.
Ⅱ.焙烧后的固体加水浸取,分离得到溶液A和固体A.
Ⅲ.向溶液A中加入醋酸调pH约7~8,分离得到溶液B和固体B.
Ⅳ.再向溶液B中继续加醋酸酸化,使溶液pH小于5.
Ⅴ.向上述溶液中加入氯化钾,得到重铬酸钾晶体.
(1)Ⅰ中焙烧发生的反应如下,配平并填写空缺:
①4FeO•Cr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2↑
②Na2CO3+Al2O3═2NaAlO2+CO2↑
(2)固体A中主要含有Fe2O3、MgO(填写化学式).
(3)已知重铬酸钾溶液中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O.Ⅳ中调节溶液pH<5时,其目的是由于存在反应平衡Cr2O72-+H2O?2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72-..
(4)Ⅴ中发生反应的化学方程式是:Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl
表是相关物质的溶解度数据:
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度 (g/100g水) | 0 | 28 | 35.7 | 4.7 | 163 |
| 40 | 40.1 | 36.4 | 26.3 | 215 | |
| 80 | 51.3 | 38 | 73 | 376 | |
②获得K2Cr2O7晶体的操作有多步组成,依次是:加入KCl固体、加热浓缩、冷却结晶、过滤、洗涤、干燥得到晶体.
(5)Ⅲ中固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析固体B中氢氧化铝含量的方法是:称取n g样品,加入过量氢氧化钠溶液(填写试剂名称)、溶解、过滤、再通入过量的CO2、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26m}{17n}$(用含m、n的代数式表示).

 ②
②
 (请用化学方程式表达).
(请用化学方程式表达). 等(任写一种).
等(任写一种).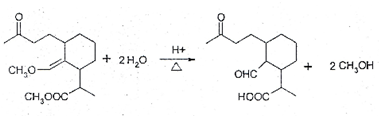 .
.