题目内容
6.下列过程:①氢氧化钠与硫酸的混合
②一氧化碳与氧气的反应
③八水合氢氧化钡与氯化铵的混合
④金属铜与硝酸银的混合
⑤浓硫酸的稀释其中(用序号填空):
(1)属于放热反应的是①②④
(2)属于吸热反应的是③,请出写出反应方程式Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
(3)能设计成原电池的反应是④,请写出正极的电极反应式Ag++e-=Ag.
分析 (1)根据常见的放热反应有:所有的物质燃烧、金属与酸或水反应、中和反应、铝热反应、绝大多数化合反应等分析;
(2)Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
(3)自发的氧化还原反应可设计成原电池,正极上发生还原反应.
解答 解:(1)①氢氧化钠与硫酸的混合是酸碱中和反应,是放热反应,
②一氧化碳与氧气的反应,所有的燃烧反应都是放热反应,
④金属铜与硝酸银的混合,是金属的置换反应,是放热反应,
故答案为:①②④;
(2)③八水合氢氧化钡与氯化铵的反应是吸热反应,化学方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
故答案为:③;Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
(3)④金属铜与硝酸银的反应是置换反应,属于氧化还原反应,可设计成原电池,正极上电解质溶液中Ag+发生还原反应,正极电极反应式为Ag++e-=Ag,
故答案为:④;Ag++e-=Ag.
点评 本题考查常见的吸热反应和放热反应类型,涉及方程式的书写和原电池中电极反应式的书写,难度不大.

练习册系列答案
相关题目
16.下列有关氮元素及其化合物的表示正确的是( )
| A. | 质子数为7、中子数为8的氮原子:${\;}_{7}^{8}$N | |
| B. | 氮原子的结构示意图: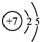 | |
| C. | 氨分子的电子式: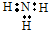 | |
| D. | 对硝基甲苯的结构简式:NO2CH3 |
17.如图所示,室温时甲、乙两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下止水夹K,使两烧瓶内气体充分接触后,容器内压强最大的是( )
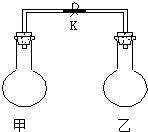
| 编号 | A | B | C | D |
| 甲中气体 | H2S | H2 | NH3 | NO |
| 乙中气体 | SO2 | Cl2 | HCl | O2 |

| A. | A | B. | B | C. | C | D. | D |
14.我国科学家成功地研制出一种长期依赖进口、价格昂贵的物质18O2.下列说法正确的是( )
| A. | 它是O3的一种同素异形体 | B. | 它是16O2的同分异构体 | ||
| C. | 18O2与16O2互为同位素 | D. | 1mol18O2分子中含有20mol电子 |
11.通常用于金属制品表面防腐的“银粉”,实际上是下列哪种金属粉末( )
| A. | Al | B. | Mg | C. | Cu | D. | Au |
18.下列分子中的各原子不可能在同一平面上的是( )
| A. | C2H4 | B. | CH3CH3 | C. | CH2═CHCl | D. | C2H2 |
15.LED系列产品是一类新型节能产品.图甲是NaBH4/H2O2燃料电池,图乙是LED发光二极管的装置示意图.下列叙述错误的是( )
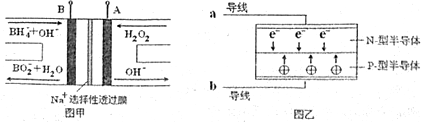

| A. | 电池A极区的电极反应式为:H2O2+2e-=2OH- | |
| B. | 电池放电过程中,Na+从负极区向正极区移动 | |
| C. | 每有1mol NaBH4参加反应转移电子数为4NA | |
| D. | 要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连 |

 ;反应类型酯化反应会取代反应;
;反应类型酯化反应会取代反应;