题目内容
10.CsICl2是一种碱金属的化合物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是( )| A. | Cs显+3价,I、Cl均显-1价 | |
| B. | 在CsICl2溶液中通入SO2气体,有硫酸生成 | |
| C. | Cs显+1价,Cl显+1价,I显-3价 | |
| D. | 在CsICl2溶液中通入Cl2,有单质碘生成 |
分析 CsICl2是一种碱金属的多卤化物,Cs为+1价,I为+1价,Cl为-1价,结合在化学反应中既可表现氧化性又可表现还原性来解答.
解答 解:A.Cs为+1价,I为+1价,Cl为-1价,故A错误;
B.CsICl2有氧化性,与具有还原性的SO2气体反应生成硫酸,故B正确;
C.Cs为+1价,I为+1价,Cl为-1价,故C错误;
D.在CsICl2溶液中通入C12,二者不反应,故D错误;
故选B.
点评 本题考查氧化还原反应,明确物质中各元素的化合价是解答本题的关键,注意化合价降低表现氧化性,化合价升高表现还原性,难度不大.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 电解质都易溶于水,所以电解质溶液导电性强 | |
| B. | 250 mL 1 mol/L的Na2SO4溶液中含有的氧原子数为NA | |
| C. | CO2通入澄清石灰水的离子反应方程式为:CO2+Ca(OH)2═CaCO3↓+H2O | |
| D. | S、Fe2+处于中间价态,既有氧化性又有还原性 |
18.下列说法正确的是( )
| A. | 物质的量是一个基本物理量,表示物质所含粒子的多少 | |
| B. | 1mol氢中含有2mol氢原子和2mol电子 | |
| C. | 1molH2O的质量等于NA 个H2O 分子的质量总和 | |
| D. | 硫酸的摩尔质量是98g |
5.下列说法正确的是( )
| A. | 20Ne和22Ne互为同位素 | B. | 石墨和金刚石是同一种物质 | ||
| C. | 氯化铵、蔗糖都属于电解质 | D. | 碘单质和碘蒸气互为同素异形体 |
15.现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来区别它们的试剂是( )
| A. | 酚酞试液 | B. | 紫色石蕊试液 | C. | AgNO3 溶液 | D. | NaHCO3溶液 |
19.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.现给出化学键的键能(见表):
请计算H2(g)+Br2(g)═2HBr(g)的反应热( )
| 化学键 | H-H | Br-Br | H-Br |
| 键能/(kJ•mol-1) | 436 | 193 | 366 |
| A. | +103 kJ•mol-1 | B. | +679 kJ•mol-1 | C. | -103 kJ•mol-1 | D. | +183 kJ•mol-1 |
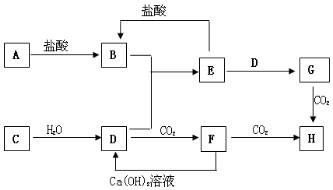 如图,图中A~H均为中学化学中常见的物质,它们之间有如下转化关系.其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应.(反应过程中生成的水及其他产物已略去)
如图,图中A~H均为中学化学中常见的物质,它们之间有如下转化关系.其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应.(反应过程中生成的水及其他产物已略去) ;F是Na2CO3.(填化学式)
;F是Na2CO3.(填化学式)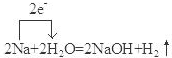 .
.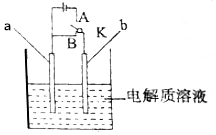 用如图所示装置进行实验,请回答下列问题:
用如图所示装置进行实验,请回答下列问题: