题目内容
下列各组溶液,无论将少量前者滴入后者,还是将少量后者滴入前者,生成物一定相同的是( )
| A、NaOH溶液和AlCl3溶液 |
| B、FeBr2溶液和氯水 |
| C、NaHCO3溶液和澄清石灰水 |
| D、Ca(HCO3)2溶液和澄清石灰水 |
考点:镁、铝的重要化合物,氯气的化学性质,钠的重要化合物
专题:元素及其化合物
分析:A、NaOH溶液和AlCl3溶液,当前者滴入后者时,后者开始足量,Al3++3OH-=Al(OH)3↓,一段时间后OH-过量,Al(OH)3+OH-=AlO2-+2H2O;当后者滴入前者时,反应方程式为:开始一段时间Al3++4OH-=AlO2-+2H2O,当Al3+过量Al3+和AlO2-发生双水解,Al3++3AlO2-+6H2O=4Al(OH)3↓;
B、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,再氧化溴离子,FeBr2溶液和氯水,当前者滴入后者时,氯水足量,同时氧化亚铁离子和溴离子,反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-;当后者滴入前者时,氯水少量,只能氧化亚铁离子,反应为2Fe2++Cl2═2Fe3++2Cl-;
C、NaHCO3溶液与澄清石灰水溶液,当前者滴入后者,发生Ca2++HCO3-+OH-═CaCO3↓+H2O;当后者滴入前者,发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-;
D、Ca(HCO3)2溶液与澄清石灰水溶液,无论前者滴入后者,还是后者滴入前者,只发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O.
B、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,再氧化溴离子,FeBr2溶液和氯水,当前者滴入后者时,氯水足量,同时氧化亚铁离子和溴离子,反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-;当后者滴入前者时,氯水少量,只能氧化亚铁离子,反应为2Fe2++Cl2═2Fe3++2Cl-;
C、NaHCO3溶液与澄清石灰水溶液,当前者滴入后者,发生Ca2++HCO3-+OH-═CaCO3↓+H2O;当后者滴入前者,发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-;
D、Ca(HCO3)2溶液与澄清石灰水溶液,无论前者滴入后者,还是后者滴入前者,只发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O.
解答:
解:A、NaOH溶液和AlCl3溶液,当前者滴入后者时,后者开始足量,Al3++3OH-=Al(OH)3↓,一段时间后OH-过量,Al(OH)3+OH-=AlO2-+2H2O,现象是先有白色沉淀后白色沉淀溶解;当后者滴入前者时,反应方程式为:开始一段时间Al3++4OH-=AlO2-+2H2O,当Al3+过量Al3+和AlO2-发生双水解,Al3++3AlO2-+6H2O=4Al(OH)3↓,现象是先无明显现象后有白色沉淀,故A错误;
B、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,再氧化溴离子,FeBr2溶液和氯水,当前者滴入后者时,氯水足量,同时氧化亚铁离子和溴离子,反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-;当后者滴入前者时,氯水少量,只能氧化亚铁离子,反应为2Fe2++Cl2═2Fe3++2Cl-,所以产物不同,故B错误;
C、NaHCO3溶液与澄清石灰水溶液,当前者滴入后者,发生Ca2++HCO3-+OH-═CaCO3↓+H2O;当后者滴入前者,发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,所以产物不同,故C错误;
D、Ca(HCO3)2溶液与澄清石灰水溶液,无论前者滴入后者,还是后者滴入前者,只发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O,无论是前者滴入后者,还是后者滴入前者,现象都是产生白色沉淀,产物一样,故D正确.
故选:D.
B、亚铁离子还原性大于溴离子,氯气先氧化亚铁离子,再氧化溴离子,FeBr2溶液和氯水,当前者滴入后者时,氯水足量,同时氧化亚铁离子和溴离子,反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-;当后者滴入前者时,氯水少量,只能氧化亚铁离子,反应为2Fe2++Cl2═2Fe3++2Cl-,所以产物不同,故B错误;
C、NaHCO3溶液与澄清石灰水溶液,当前者滴入后者,发生Ca2++HCO3-+OH-═CaCO3↓+H2O;当后者滴入前者,发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,所以产物不同,故C错误;
D、Ca(HCO3)2溶液与澄清石灰水溶液,无论前者滴入后者,还是后者滴入前者,只发生Ca2++2HCO3-+2OH-═CaCO3↓+2H2O,无论是前者滴入后者,还是后者滴入前者,现象都是产生白色沉淀,产物一样,故D正确.
故选:D.
点评:本题考查离子反应的书写,明确反应是解答本题的关键,注意互滴顺序不同发生的反应与现象的关系即可解答,题目难度较大.

练习册系列答案
相关题目
实验是化学研究的基础.下列关于各实验装置的叙述正确的是( )


| A、装置①常用于分离乙醇或苯等与水组成的混合物 |
| B、装置②可用于吸收NH3或HCl气体,并防止倒吸 |
| C、装置③可用于收集H2、CO2、Cl2、NO等气体 |
| D、装置④可用于干燥、收集氨气,并吸收多余的氨气 |
下列实验过程中会先产生白色沉淀后沉淀又溶解的是( )
| A、向AlCl3溶液中滴加氨水至过量 |
| B、向Ba(NO3)2溶液通入SO2至过量 |
| C、向Ba(0H)2溶液通入CO2至过量 |
| D、向新制Fe(OH)3胶体中滴加稀硫酸至过量 |
常温时,下列关于溶液的pH或微粒的物质的量浓度的说法不正确的是( )
| A、将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3?H2O) |
| B、某溶液中只存在Cl-、OH、NH4+、H+四种离子,则一定不存在下列关系:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C、将0.2 mol?L-1的某一元酸HA溶液和0.1 mol?L-1NaOH溶液等体积混合后,溶液pH大于7,则反应后的混合液中:2c(OH-)+c(A-)=2c(H+)+c(HA) |
| D、某物质的溶液中由水电离出的c(H+)=1×10-amol?L-1,则溶液的pH一定为14-a |
常温下,下列各组离子或分子在指定溶液中能大量共存的是( )
| A、氨水中:NH4+、Fe2+、SO42-、HSO3- |
| B、pH=l的溶液中:Mg2+、Fe3+、Cl-、NO3- |
| C、通入足量CO2的溶液中:Ca2+、Na+、CO32-、SiO32- |
| D、水电离产生的c(H+)=1×10-14 mol?L-1的溶液中:Al3+、K+、Cl、CH3COO- |
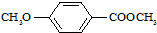
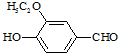 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.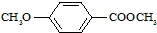 )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( 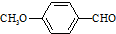 )合成X.用反应流程图表示如下:
)合成X.用反应流程图表示如下: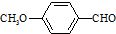 →
→
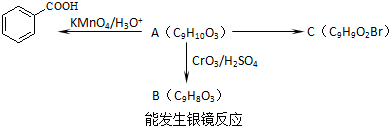
 如图为10mL一定物质的量浓度的盐酸(HCl),用一定浓度的NaOH溶液滴定的图示,依据图示推出HCl和NaOH的物质的量浓度是( )
如图为10mL一定物质的量浓度的盐酸(HCl),用一定浓度的NaOH溶液滴定的图示,依据图示推出HCl和NaOH的物质的量浓度是( )