题目内容
下列图示与对应的叙述相符的是( )
A、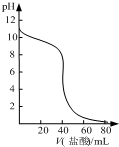 如图表示盐酸滴加到0.1mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B、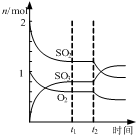 如图表示一定条件下进行的反应2SO2+O2═2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
C、 如图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
D、 如图表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
考点:中和滴定,物质的量或浓度随时间的变化曲线,弱电解质在水溶液中的电离平衡
专题:图示题
分析:A.碱溶液pH<13,说明是弱碱溶液;
B.图中表示t2时改变条件,平衡正向移动;
C.20mL Ba(OH)2溶液时,铝离子恰好变成AlO2-;
D.稀释醋酸促进电离,pH变化小.
B.图中表示t2时改变条件,平衡正向移动;
C.20mL Ba(OH)2溶液时,铝离子恰好变成AlO2-;
D.稀释醋酸促进电离,pH变化小.
解答:
解:A.图示表示的碱溶液pH<13,说明是弱碱溶液;反应后是强酸弱碱溶液,宜选择酸性变色突变的甲基橙,而不是碱性变色突变的酚酞作指示剂,故A错误;
B.t2时改变条件,平衡正向移动,可能是加压过程,故B正确;
C.明矾溶液中加入Ba(OH)2溶液的拐点方程式是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4、KAl(SO4)2+2Ba(OH)2═KAlO2+2BaSO4↓+2H2O,同样2mol KAl(SO4)2,按前者反应产生的沉淀质量是(2×78+3×233)g=855g,按后者反应产生的沉淀质量是4×233g=932g,图象形态正确,20mL Ba(OH)2溶液时,铝离子恰好变成AlO2-,故C错误;
D.盐酸与醋酸的稀释,pH变化大的是盐酸,故D错误.
故选B.
B.t2时改变条件,平衡正向移动,可能是加压过程,故B正确;
C.明矾溶液中加入Ba(OH)2溶液的拐点方程式是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4、KAl(SO4)2+2Ba(OH)2═KAlO2+2BaSO4↓+2H2O,同样2mol KAl(SO4)2,按前者反应产生的沉淀质量是(2×78+3×233)g=855g,按后者反应产生的沉淀质量是4×233g=932g,图象形态正确,20mL Ba(OH)2溶液时,铝离子恰好变成AlO2-,故C错误;
D.盐酸与醋酸的稀释,pH变化大的是盐酸,故D错误.
故选B.
点评:本题以图象题的形式呈现来考查知识点,做题时要注意从图象中获取正确信息,正确判断得出结论.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质中属于非电解质的是( )
| A、NaOH |
| B、CO2 |
| C、H2SO4 |
| D、Fe |
下列反应的离子方程式书写正确的是( )
| A、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B、稀H2SO4与铁粉反应:Fe+4H+=Fe3++2H2↑ |
| C、氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D、三氧化二铁与稀盐酸混合:Fe2O3+6H+=Fe3++3H2O |
下列反应属于离子反应的是( )
| A、锌片放入稀H2SO4中 |
| B、H2和O2反应生成水 |
| C、KMnO4加热分解制O2 |
| D、用H2还原灼热的CuO |
用标准盐酸滴定未知浓度的NaOH溶液时,若测定结果偏高,则产生误差的原因可能是( )
| A、滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗 |
| B、酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C、滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D、配置NaOH溶液时,NaOH固体中混有少量KOH固体 |
下列说法不正确的是( )
| A、热水瓶胆中的水垢可以用食醋除去 |
| B、可以用淀粉溶液检验加碘盐中是否含碘元素 |
| C、在蔗糖中加入浓硫酸出现黑色物质,说明浓硫酸具有脱水性 |
| D、做红烧鱼时,常加一些食醋和酒会更香,是因为生成少量的酯 |
等体积、等浓度的HCOONa和NaCN溶液,溶液中离子总数的关系正确的是(已知HCOOH比HCN易电离)( )
| A、HCOONa=NaCN |
| B、HCOONa>NaCN |
| C、HCOONa<NaCN |
| D、无法确定 |