题目内容
某无色透明溶液,只可能含下列离子:Mg2+、Cu2+、Ba2+、H+、SO42-、SO32-、HCO3-、OH -、NO3-.该溶液能跟金属铝反应放出H2,试判断何者能大量存在于此溶液中?
(1)当生成Al3+时,可能存在 .
(2)当生成AlO2-时,可能存在 .
(1)当生成Al3+时,可能存在
(2)当生成AlO2-时,可能存在
考点:离子共存问题,铝的化学性质
专题:离子反应专题,几种重要的金属及其化合物
分析:该溶液能跟金属铝反应放出H2,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:该溶液能跟金属铝反应放出H2,为非氧化性酸或强碱溶液,
(1)当生成Al3+时,溶液显酸性,与氢离子反应的不能存在SO32-、HCO3-、OH -,且Al、NO3-发生氧化还原反应不能生成氢气,Cu2+为蓝色,由电荷守恒可知阴离子一定存在SO42-,则不能存在Ba2+,可存在的离子为Mg2+、H+、SO42-,故答案为:Mg2+、H+、SO42-;
(2)当生成AlO2-时,溶液显碱性,与氢氧根离子反应的Mg2+、Cu2+、H+、HCO3-不能存在,由电荷守恒可知一定存在Ba2+,则与Ba2+反应的SO42-、SO32-不能存在,则溶液中可存在Ba2+、OH -、NO3-,
故答案为:Ba2+、OH -、NO3-.
(1)当生成Al3+时,溶液显酸性,与氢离子反应的不能存在SO32-、HCO3-、OH -,且Al、NO3-发生氧化还原反应不能生成氢气,Cu2+为蓝色,由电荷守恒可知阴离子一定存在SO42-,则不能存在Ba2+,可存在的离子为Mg2+、H+、SO42-,故答案为:Mg2+、H+、SO42-;
(2)当生成AlO2-时,溶液显碱性,与氢氧根离子反应的Mg2+、Cu2+、H+、HCO3-不能存在,由电荷守恒可知一定存在Ba2+,则与Ba2+反应的SO42-、SO32-不能存在,则溶液中可存在Ba2+、OH -、NO3-,
故答案为:Ba2+、OH -、NO3-.
点评:本题考查离子的共存,为高频考点,把握习题中的信息、溶液的酸碱性及常见离子之间的反应为解答的关键,注意(1)中硝酸根离子判断为解答的易错点,题目难度不大.

练习册系列答案
相关题目
下列事实与胶体性质无关的是( )
| A、明矾可用来净水 |
| B、一束平行光线照射蛋白质溶液时,从一侧可以看到光亮的通路 |
| C、FeCl3溶液中滴入NaOH溶液,出现红褐色沉淀 |
| D、Al(OH)3或Fe(OH)3胶体可以吸附水中的悬浮颗粒而沉降 |

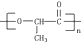 由一种单体缩聚而成的,该单体的结构简式为
由一种单体缩聚而成的,该单体的结构简式为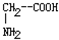 和丙氨酸
和丙氨酸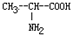 混合反应,生成的“二肽”最多为
混合反应,生成的“二肽”最多为