题目内容
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.那么( )
| A、NH4HCO3和醋酸溶液不能发生反应 |
| B、0.1mol NH4HCO3粉末中NH4+和HCO3-总数小于1.204×1023 |
| C、醋酸凝固时释放的能量储存于NH4Cl、CO2和H2O中 |
| D、如果改加体积和pH值均与盐酸相同的稀硫酸,可能不会发生上述现象 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:反应过程中醋酸逐渐凝固,说明HCl和NH4HCO3反应过程中温度降低,则该反应是吸热反应,
A.醋酸酸性大于碳酸,NH4HCO3和醋酸溶液能反应;
B.碳酸氢铵的构成微粒是铵根离子和碳酸氢根离子;
C.醋酸凝固时会释放能量,HCl和NH4HCO3反应吸收能量;
D.稀硫酸和盐酸都具有酸性,都能和碳酸氢铵反应.
A.醋酸酸性大于碳酸,NH4HCO3和醋酸溶液能反应;
B.碳酸氢铵的构成微粒是铵根离子和碳酸氢根离子;
C.醋酸凝固时会释放能量,HCl和NH4HCO3反应吸收能量;
D.稀硫酸和盐酸都具有酸性,都能和碳酸氢铵反应.
解答:
解:反应过程中醋酸逐渐凝固,说明HCl和NH4HCO3反应过程中温度降低,则该反应是吸热反应,
A.醋酸酸性大于碳酸,根据强酸制取弱酸知,NH4HCO3和醋酸溶液能反应,故A错误;
B.碳酸氢铵的构成微粒是铵根离子和碳酸氢根离子,所以0.1mol NH4HCO3粉末中NH4+和HCO3-总数等于1.204×1023,故B错误;
C.醋酸凝固时会释放能量,HCl和NH4HCO3反应吸收能量,所以醋酸凝固时释放的能量储存于NH4Cl、CO2和H2O中,故C正确;
D.稀硫酸和盐酸都具有酸性,都能和碳酸氢铵反应,且HCl和硫酸都是强电解质,所以如果改加体积和pH值均与盐酸相同的稀硫酸,可能会发生上述现象,故D错误;
故选C.
A.醋酸酸性大于碳酸,根据强酸制取弱酸知,NH4HCO3和醋酸溶液能反应,故A错误;
B.碳酸氢铵的构成微粒是铵根离子和碳酸氢根离子,所以0.1mol NH4HCO3粉末中NH4+和HCO3-总数等于1.204×1023,故B错误;
C.醋酸凝固时会释放能量,HCl和NH4HCO3反应吸收能量,所以醋酸凝固时释放的能量储存于NH4Cl、CO2和H2O中,故C正确;
D.稀硫酸和盐酸都具有酸性,都能和碳酸氢铵反应,且HCl和硫酸都是强电解质,所以如果改加体积和pH值均与盐酸相同的稀硫酸,可能会发生上述现象,故D错误;
故选C.
点评:本题考查了物质构成、化学反应能量变化等知识点,利用能量守恒定律正确理解题干信息是解本题关键,知道醋酸凝固原因,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
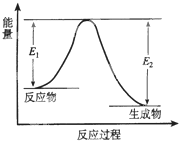 反应A(g)+B(g)?C(g)+D(g) 发生过程中的能量变化如右图,△H 表示反应的焓变.下列说法正确的是( )
反应A(g)+B(g)?C(g)+D(g) 发生过程中的能量变化如右图,△H 表示反应的焓变.下列说法正确的是( )| A、该反应为吸热反应 |
| B、反应体系中加入催化剂,反应速率增大,E1减小,E2增大 |
| C、反应体系中加入催化剂,反应速率增大,△H不变 |
| D、反应达到平衡时,降低温度,A的转化率增大 |
下列有关同分异构体数目的叙述中,正确的是( )
| A、C5H12有2种同分异构体 |
| B、C8H10中只有三种属于芳香烃的同分异构体 |
| C、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| D、CH3CH2CH2CH3光照下与氯气反应,只生成一种一氯代烃 |
能正确表示下列反应的离子方程式是( )
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ |
| B、碳酸钠溶液中加入少量稀盐酸 2 H++CO32-=CO2↑+H2O |
| C、用FeCL3溶液腐蚀铜板制印刷电路 2Fe3++Cu=2Fe2++Cu2+ |
| D、稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑ |
下列说法中不正确的是( )
| A、Na,Mg,Al金属性依次减弱 |
| B、HCl,H2S,PH3稳定性依次减弱 |
| C、NaOH,KOH,CsOH碱性依次减弱 |
| D、S2-,Cl-,Ca2+半径依次减小 |
下列说法正确的是( )
| A、族序数等于其周期序数的元素一定是金属元素 |
| B、13C与14C互为同位素,它们的化学性质相同,但相对原子质量不同 |
| C、元素原子的最外层电子数等于元素的最高化合价 |
| D、全部由非金属元素组成的化合物中只含共价键 |
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
| A、c(NH4+):③>② |
| B、pH:①>②>③ |
| C、Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)向溶解方向移动 |
| D、等体积①和③混合溶液中 c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-) |
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②AgNO3③(NH4)2S ④HOOC-COONa⑤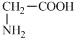 ⑥
⑥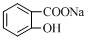
①NaHCO3 ②AgNO3③(NH4)2S ④HOOC-COONa⑤
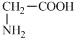 ⑥
⑥
| A、全部 | B、①②④⑤⑥ |
| C、②③④⑤⑥ | D、②④⑤⑥ |



