题目内容
13.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到.现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液.①电解开始不久,阴极产生的实验现象有产生气泡,溶液变红,阴极的电极反应是2H2O+2e-=H2↑+2OH-.
②阳极区溶液变蓝色,同时伴随的现象还有产生白色沉淀、铜片溶解,对阳极区溶液呈蓝色的正确解释是C.
A.2I--2e-=I2;碘遇淀粉变蓝
B.Cu-2e-=Cu2+;Cu2+显蓝色
C.2Cu+4I--4e-=2CuI↓+I2; 碘遇淀粉变蓝
D.4OH--4e-=2H2O+O2;O2将I-氧化为I2,碘遇淀粉变蓝.
分析 石墨为阴极,以Cu为阳极电解KI溶液,通电后,溶液中的H+、K+移向阴极,而H+的氧化性强于K+,所以H+得电子被还原,电极反应式为2H2O+2e-=H2↑+2OH-,破坏了水的电离平衡,使c(OH-)>c(H+),酚酞试液变红;I-和OH-移向阳极,而失电子能力Cu>I->OH-,故Cu失电子产生Cu2+,生成的Cu2+和碘离子发生氧化还原反应生成碘单质.
解答 解:①石墨为阴极,以Cu为阳极电解KI溶液,通电后,溶液中的H+、K+移向阴极,而H+的氧化性强于K+,所以在阴极上H+得电子被还原,电极反应式为2H2O+2e-=H2↑+2OH-,破坏了水的电离平衡,使c(OH-)>c(H+),溶液呈碱性,则酚酞试液变红,
故答案为:产生气泡,溶液变红; 2H2O+2e-=H2↑+2OH-;
②I-和OH-移向阳极,而失电子能力Cu>I->OH-,故Cu失电子产生Cu2+,生成的Cu2+和碘离子发生氧化还原反应生成碘单质,反应方程式为2Cu+4I--4e-=2CuI↓+I2,生成的碘遇淀粉试液变蓝色,所以阳极区产生白色沉淀、铜片溶解、溶液呈蓝色.
故答案为:产生白色沉淀、铜片溶解;C.
点评 本题考查电解原理,明确离子放电顺序及电极材料是解本题关键,活泼金属作阳极时,阳极上金属失电子而不是溶液中阴离子放电,为易错点.

练习册系列答案
相关题目
10.下列事实与胶体性质无关的是( )
| A. | 向豆浆中加入硫酸钙做豆腐 | |
| B. | 将植物油倒入水中用力搅拌形成油水混合物 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | 观看电影时,从放映机到银幕有明显的光路 |
1.下列仪器用于过滤和蒸发分离物质的是( )
①漏斗 ②试管 ③蒸发皿 ④天平 ⑤烧杯 ⑥研钵.
①漏斗 ②试管 ③蒸发皿 ④天平 ⑤烧杯 ⑥研钵.
| A. | ①③④ | B. | ①②⑥ | C. | ①③⑤ | D. | ①③⑥ |
8.下列有关环境问题的说法正确的是( )
| A. | 燃煤时加入适量石灰石,可减少废气中SO2的量 | |
| B. | 臭氧的体积分数超过10-4%的空气有利于人体健康 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 含磷合成洗涤剂易于被细菌分解,故不会导致水体污染 |
5.下列有关胶体的叙述正确的是( )
| A. | Fe(OH)3胶体有丁达尔效应是Fe(OH)3胶体区别于FeCl3溶液最本质的特征 | |
| B. | 阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现 | |
| C. | 鸡蛋清溶液分类上属于悬浊液 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体 |
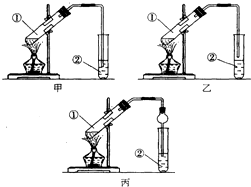 下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.