题目内容
当不慎有大量氯气逸出周围空间时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是( )
| A、NaOH |
| B、NaCl |
| C、醋酸 |
| D、Na2CO3 |
考点:氯气的化学性质
专题:卤族元素
分析:氯气是有毒气体,氯气和水反应生成盐酸和次氯酸,盐酸能和碱性物质反应,由于碱性物质与人体皮肤接触,所以不能用强碱性物质,则该溶液应该具有弱碱性、腐蚀性弱的特点,据此分析解答.
解答:
解:A.NaOH虽能与氯气反应,达到吸收氯气的效果,但NaOH的腐蚀性强,不能用浸有浓NaOH溶液的毛巾捂住鼻子,故A错误;
B.食盐中含有氯离子,抑制氯气溶解,但不能吸收氯气,故B错误;
C.醋酸抑制氯气的溶解,不能吸收氯气,故C错误;
D.Na2CO3溶液显碱性,能与氯气反应而防止吸入氯气中毒,则可以用浸有Na2CO3溶液的毛巾捂住鼻子,故D正确.
故选D.
B.食盐中含有氯离子,抑制氯气溶解,但不能吸收氯气,故B错误;
C.醋酸抑制氯气的溶解,不能吸收氯气,故C错误;
D.Na2CO3溶液显碱性,能与氯气反应而防止吸入氯气中毒,则可以用浸有Na2CO3溶液的毛巾捂住鼻子,故D正确.
故选D.
点评:本题考查了氯气的性质,明确氯气和水反应的生成物及其性质是解本题关键,注意氯化钠溶液中含有氯离子,氯气和水反应生成盐酸,所以氯化钠溶液抑制氯气溶解,实验室可以采用排饱和食盐水方法除去氯气中的氯化氢气体,难度不大.

练习册系列答案
相关题目
已知某乳制品中富含钙元素,则下列食品中也富含钙元素的是( )
| A、水果 | B、动物肝脏 |
| C、海带 | D、豆类 |
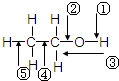 乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明正确的是
乙醇分子中各化学键如图所示,对乙醇在各种反应中断裂的键说明正确的是( )
| A、和金属钠作用时,键②断裂 |
| B、和浓硫酸共热至170℃时,键①和⑤断裂 |
| C、和乙酸、浓硫酸共热时,键①断裂 |
| D、在铜催化下和氧气反应时,键①和②断裂 |
下列所示的实验装置中,能达到实验目的是( )
A、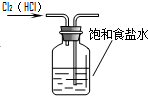 除去Cl2中的HCl |
B、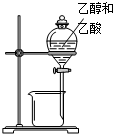 分离乙醇和乙酸 |
C、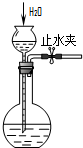 检查装置气密性 |
D、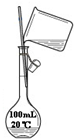 配制150 mL 0.10 mol?L-1盐酸 |
下列溶液:①CH3COOH ②HCl ③NaOH ④CH3COONa ⑤KCl ⑥NH4Cl其物质的量浓度均为0.1mol/L,其pH由小到大排列顺序为( )
| A、③④⑤⑥①② |
| B、④⑤⑥①③② |
| C、②①⑥⑤④③ |
| D、②③①⑥⑤④ |
 A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空:
A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空: