题目内容
6.下列有关物质检验的实验结论正确的是( )| 实 验 操 作 | 现 象 | 实 验 结 论 | |
| A | 向某溶液中加入硝酸酸化的氯化钡溶液 | 生成白色沉淀 | 溶液中一定含有SO42- |
| B | 将某溶液蘸取少量放置于火焰上灼烧 | 火焰呈黄色 | 该溶液中一定含K+ |
| C | 往某溶液中加入KSCN溶液 | 显血红色 | 溶液中一定含有Fe3+ |
| D | 往某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO32- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向某溶液中加入硝酸酸化的氯化钡溶液,可能生成AgCl、BaSO4等沉淀;
B.根据钠离子、钠离子的焰色反应的火焰颜色判断;
C.三价铁离子遇到硫氰酸钾显示红色;
D.能和盐酸反应产生二氧化碳气体的离子可以是碳酸根离子还可以是碳酸氢根离子.
解答 解:A.向某溶液中加入硝酸酸化的氯化钡溶液,生成白色沉淀,不一定是SO42-,如果溶液中含有SO32-,能被氧化为SO42-,也不能排除生成AgCl沉淀,应先加盐酸酸化,如无沉淀,再加入氯化钡观察,故A错误;
B.将某溶液蘸取少量放置于火焰上灼烧,火焰呈黄色,说明溶液中一定含有Na+,故B错误;
C.因Fe3+与SCN-发生反应:Fe3++3SCN-=Fe(SCN)3,溶液呈血红色,所以溶液中滴入KSCN溶液后变红,说明该溶液中含有Fe3+,故C正确;
D.某溶液加入足量盐酸,放出的气体能使澄清石灰水变浑浊,该气体是二氧化碳或是二氧化硫,该溶液中含有CO32-、SO32-、HCO3-中的至少一种离子,故D错误;
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,注意检验离子的存在情况时,需要排除干扰离子,确保检验方案的严密性.

练习册系列答案
相关题目
14.如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
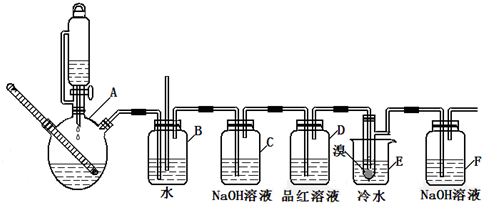
有关数据如表:
请按要求回答下列问题:
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)下列有关A中反应说法错误的是AD(填编号)
A.将乙醇缓慢加入浓硫酸中配制混合酸
B.温度在140℃时,其主要反应为取代反应
C.浓硫酸的作用是脱水和催化
D.加入碎瓷片的作用是加快反应速度
(3)装置D中品红溶液的作用是验证二氧化硫是否被除尽;同时B装置是安全瓶,监测实验进行时E中是否发生堵塞,请写出堵塞时的现象玻璃管中液面上升.
(4)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发,但又不能用冰水,其原因是1,2-二溴乙烷易凝结成固体而发生堵塞.
(5)装置F中的化学反应方程式为:Br2+2NaOH=NaBr+NaBrO+H2O.

有关数据如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)下列有关A中反应说法错误的是AD(填编号)
A.将乙醇缓慢加入浓硫酸中配制混合酸
B.温度在140℃时,其主要反应为取代反应
C.浓硫酸的作用是脱水和催化
D.加入碎瓷片的作用是加快反应速度
(3)装置D中品红溶液的作用是验证二氧化硫是否被除尽;同时B装置是安全瓶,监测实验进行时E中是否发生堵塞,请写出堵塞时的现象玻璃管中液面上升.
(4)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发,但又不能用冰水,其原因是1,2-二溴乙烷易凝结成固体而发生堵塞.
(5)装置F中的化学反应方程式为:Br2+2NaOH=NaBr+NaBrO+H2O.