题目内容
下列有关化学表达正确的是( )
A、CS2的比例模型: |
B、铍原子最外层的电子云图: |
C、乙醇的球棍模型: |
D、氮原子最外层轨道表示式: |
考点:球棍模型与比例模型,原子核外电子排布
专题:化学用语专题,原子组成与结构专题
分析:A、比例模型中用不同体积的小球表示不同原子的大小,二硫化碳中硫原子的原子半径大于碳原子;
B、铍原子最外层为s能级,s能级的电子云图为球形;
C、乙醇分子中含有6个氢原子,图示结构中只含有4个氢原子;
D、氮原子最外层5个电子,图示为氮原子所有核外电子排布.
B、铍原子最外层为s能级,s能级的电子云图为球形;
C、乙醇分子中含有6个氢原子,图示结构中只含有4个氢原子;
D、氮原子最外层5个电子,图示为氮原子所有核外电子排布.
解答:
解:A、二硫化碳中硫原子的原子半径大于碳原子,CS2的比例模型为: ,故A正确;
,故A正确;
B、铍原子最外层为s能级,s能级的电子云图为球形: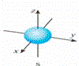 ,故B错误;
,故B错误;
C、 中含有4个氢原子,而乙醇分子中含有6个氢原子,所以乙醇的球棍模型为:
中含有4个氢原子,而乙醇分子中含有6个氢原子,所以乙醇的球棍模型为: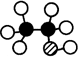 ,故C错误;
,故C错误;
D、氮原子最外层5个电子,其最外层轨道表示式为: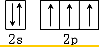 ,故D错误;
,故D错误;
故选A.
 ,故A正确;
,故A正确;B、铍原子最外层为s能级,s能级的电子云图为球形:
 ,故B错误;
,故B错误;C、
 中含有4个氢原子,而乙醇分子中含有6个氢原子,所以乙醇的球棍模型为:
中含有4个氢原子,而乙醇分子中含有6个氢原子,所以乙醇的球棍模型为: ,故C错误;
,故C错误;D、氮原子最外层5个电子,其最外层轨道表示式为:
 ,故D错误;
,故D错误;故选A.
点评:本题考查了球棍模型与比例模型、原子核外电子排布,题目难度中等,注意明确球棍模型和比例模型的表示方法,掌握原子核外电子排布的表示方法.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、用Na2CO3溶液作洗涤剂:CO-23+H2O?HCO-3+OH- | ||||
B、用氯气给自来水消毒:Cl2+H2O
| ||||
| C、电解饱和食盐水制烧碱:2Cl-+2H2O═Cl2↑+H2↑+2OH- | ||||
| D、Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O |
下列叙述及对应的离子方程式均正确的是( )
| A、用Cu除去FeCl2溶液中少量的FeCl3杂质:Cu+2Fe3+═Cu2++2Fe2+ |
| B、工业上用NO2与水反应制取HNO3:3NO2+H2O═NO3-+NO+2H+ |
| C、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O |
| D、硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、2g H2所含有的原子数目是NA |
| C、18g H2O在标准状况下的体积是22.4L |
| D、在标准状况时,20mL NH3与60mL O2所含的分子个数比为2:1 |
等质量的镁分别在①O2 ②N2 ③CO2 ④空气中充分燃烧,产物中固体的质量从大到小的顺序是( )
| A、①=③>②=④ |
| B、③>①>④>② |
| C、①=③>④>② |
| D、②>④>③>① |