题目内容
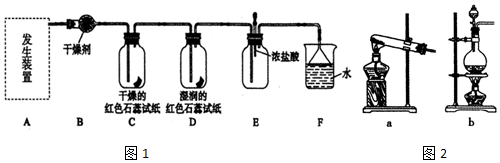
12.工业上曾用电解60%硫酸溶液(或硫酸氢钾、硫酸氢铵浓溶液)制取过氧化氢,其生产流程如图:
下列说法错误的是( )
| A. | 电解硫酸或酸式硫酸盐溶液,阳极反应为2SO42--2e-═S2O82- | |
| B. | S2O82-具有强氧化性,H2S2O8是二元强酸 | |
| C. | 减压蒸馏的目的是为了减少H2O2分解,蒸馏得到的另一组分可循环利用 | |
| D. | 由溶液A转化为溶液B发生了氧化还原反应 |
分析 用惰性电极电解60%的硫酸溶液,得到溶液A中含有H+、S2O82-存在-O-O-键,S元素化合价仍为+6价,但O元素化合价为-1价,说明SO42-被氧化,为电解池的阳极反应,由溶液A生成B溶液生成H2O2、H+、SO42-,S2O82-发生水解反应生成SO42-,同时生成H2O2,减压蒸馏,可得到H2O2的浓溶液,以此解答该题.
解答 解:A.阳极发生氧化反应,SO42-被氧化,电极方程式为2SO42--2e-═S2O82-,故A正确;
B.S2O82-存在-O-O-键,具有强氧化性,A中含有H+、S2O82-,说明H2S2O8是二元强酸,故B正确;
C.过氧化氢不稳定,易分解,减压蒸馏可减小沸点,避免分解,蒸馏得到的另一组分含有H+、SO42-,可循环利用,故C正确;
D.由溶液A转化为溶液B,S2O82-水解反应SO42-和H2O2,为非氧化还原反应,故D错误.
故选D.
点评 本题考查物质的制备以及分离,为高频考点,侧重考查学生的分析能力和实验能力,注意把握电解的规律和应用,易错点为D,注意S2O82-存在-O-O-键,S2O82-水解反应SO42-和H2O2,为易错点,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合质子能力最强的是CO32-.
②根据表中数据判断,浓度均为0.01mol•L-1的下列四种物质的溶液中,酸性最强的是D;将各溶液分别稀释100倍,pH变化最小的是A(填编号).
A.HCN B.HClO C.H2CO3 D.CH3COOH
③据上表数据,请你判断下列反应不能成立的是C(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO.
(2)已知常温下Cu(OH)2的Ksp=2×10-20.又知常温下某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于5;要使0.2mol•L-1的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH为6.
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
②根据表中数据判断,浓度均为0.01mol•L-1的下列四种物质的溶液中,酸性最强的是D;将各溶液分别稀释100倍,pH变化最小的是A(填编号).
A.HCN B.HClO C.H2CO3 D.CH3COOH
③据上表数据,请你判断下列反应不能成立的是C(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO.
(2)已知常温下Cu(OH)2的Ksp=2×10-20.又知常温下某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于5;要使0.2mol•L-1的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH为6.
3.下列有关物质的性质与用途具有对应关系的是( )
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4Cl受热易分解,可用作氮肥 | |
| C. | MgO熔点高,可用作耐高温材料 | |
| D. | KAl(SO4)2•12H2O易溶于水,可用作净水剂 |
17.用NA表示阿伏伽德罗常数,下列叙述中正确的是( )
| A. | 12g 12C含中子数为NA | |
| B. | 标准状况下,22.4L氖气中含有原子数为2NA | |
| C. | 28g CO和N2混合气体含有的原子数为2NA | |
| D. | 2mol钠与足量O2完全反应生成Na2O2时失去电子数为NA |
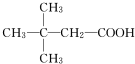
4. 某有机物的结构为如图所示,这种有机物不可能具有的性质是( )
某有机物的结构为如图所示,这种有机物不可能具有的性质是( )
①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生水解反应.
 某有机物的结构为如图所示,这种有机物不可能具有的性质是( )
某有机物的结构为如图所示,这种有机物不可能具有的性质是( )①可以燃烧;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生水解反应.
| A. | ①④ | B. | 只有⑤ | C. | ②⑤ | D. | ④⑤ |
2.Al可以与稀硝酸反应,已知HNO3被还原为N2O.若标准状况有3.36LN2O生成.则参加反应的Al的质量(g)为( )
| A. | 27 | B. | 5.4 | C. | 10.8 | D. | 16.2 |


 .(用结构简式表示)
.(用结构简式表示)