题目内容
13.利用如图所示的装置进行实验,若装置Ⅰ中反应物充足,则装置Ⅱ中实验现象正确的是( )| 选项 | ① | ② | ③ | Ⅱ中的现象 | 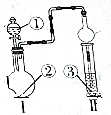 |
| A | 浓盐酸 | 碳酸钙 | 滴有酚酞的稀碳酸钠溶液 | 溶液由红色最终变为浅红色 | |
| B | 浓氨水 | 氧化钙 | 氯化铝溶液 | 先产生白色沉淀,后沉淀溶解 | |
| C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 | |
| D | 浓硝酸 | 铜 | 硅酸钠溶液 | 有胶状物生成 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.反应生成二氧化碳气体,且盐酸易挥发,二氧化碳、盐酸均与碳酸钠反应;
B.反应生成氨气,氨气与氯化铝反应生成氢氧化铝沉淀;
C.酯化反应需要加热;
D.反应生成二氧化氮,且硝酸易挥发,与硅酸钠溶液发生复分解反应生成硅酸.
解答 解:A.反应生成二氧化碳气体,且盐酸易挥发,二氧化碳、盐酸均与碳酸钠反应,则碱性减弱,观察到Ⅱ中溶液由红色最终变为无色,故A错误;
B.反应生成氨气,氨气与氯化铝反应生成氢氧化铝沉淀,则观察到Ⅱ中只生成白色沉淀,不能溶解,故B错误;
C.酯化反应需要加热,则图中装置不能生成乙酸乙酯,故C错误;
D.反应生成二氧化氮,且硝酸易挥发,与硅酸钠溶液发生复分解反应生成硅酸,则观察到Ⅱ中出现胶状物,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验装置的作用、气体的制备原理等为解答的关键,侧重分析与实验能力的考查,注意反应原理的应用及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
3.下列物质既能与稀硫酸反应,又有跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Na2CO3 ③Al2O3 ④Al(OH)3 ⑤Al.
①NaHCO3 ②Na2CO3 ③Al2O3 ④Al(OH)3 ⑤Al.
| A. | ③④ | B. | ②④⑤ | C. | ①③④⑤ | D. | 全部 |
4.下列说法,错误的是( )
| A. | 乙醇俗称酒精 | B. | 无水乙酸又称冰醋酸 | ||
| C. | 乙酸和乙醇可以发生酯化反应 | D. | 葡萄糖不是有机物 |
1.下列实验能获得成功的是( )
| A. | 用水鉴别乙醇和乙酸 | |
| B. | 将甲烷通入氯水中生成一氯甲烷 | |
| C. | 在苯中滴入稀硝酸制硝基苯 | |
| D. | 用食醋浸泡有水垢的水壶清除其中的水垢 |
8.下列物质中,不属于卤代烃的是( )
| A. | 氯乙烯 | B. | 溴苯 | C. | 四氯乙烯 | D. | 二氧化硅 |
7.在室温下进行中和滴定,酸和碱恰好完全反应时,以下说法一定正确的是( )
| A. | 能用适当的酸碱指示剂来判断 | |
| B. | 参加反应的酸中的H+离子总量和碱中OH-离子总量相等 | |
| C. | 反应混合液的pH=7 | |
| D. | 反应的热效应即为中和热 |
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA | |
| C. | 加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子 | |
| D. | 0.1mol Na2O2与足是的潮湿的二氧化碳反应转移的电子数为0.1NA |