题目内容
(12分)亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组拟制备NaNO2并测定产品纯度。
I【查阅资料】
①2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
②NO能被酸性高锰酸钾氧化成NO2。
③酸性条件下MnO4-被还原为Mn2+。
Ⅱ【制备产品】
用如下装置制NaNO2(夹持和加热装置已省略)。
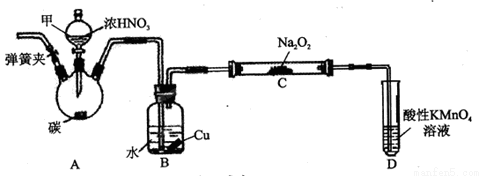
(1)装置A烧瓶中发生反应的化学方程式为_______________________。
(2)B装置的作用是_________________________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为排除干扰应在B、C装置间增加装置E,E中盛放的试剂可能是_________。(填字母编号)
A.浓H2SO4 B.碱石灰 C.无水CaCl2 D.生石灰
Ⅲ【测定纯度】.
设计如下方案测定产品的纯度。

(4)溶液A到溶液B发生反应的离子方程式为____________________________。
(5)取样品2.3g经一系列操作后得到溶液A100mL,准确量取10.00mL A与24.00mL 0.05mol/L的酸性KMnO4溶液在锥形瓶中充分反应。反应后溶液用0.1 mol/L(NH4)2Fe(SO4)2标准溶液滴定至紫色刚好褪去;重复上述实验2次,平均消耗(NH4)2 Fe(SO4)2溶液10.00ml,则样品中NaNO2的纯度为__________。
Ⅳ【探究反思】
(6)NaNO2的纯度偏低,该小组讨论提出的原因中可能正确的是________。(填字母编号)
A.滴定至溶液紫色刚好褪去就立刻停止滴加
B.加入A与KMnO4溶液前锥形瓶未经干燥
C.实验中使用的(NH4)2 Fe(SO4)2溶液暴露在空气中时间过长
(1)C+4HNO3(浓)  CO2↑+4NO2↑+2H2O;(2)将NO2转化为NO,同时铜与稀硝酸反应生成NO;(3)B、D;(4)2MnO4-+5NO2-+6H+=2Mn2++3H2O+5NO3-;(5)75%;(6)C。
CO2↑+4NO2↑+2H2O;(2)将NO2转化为NO,同时铜与稀硝酸反应生成NO;(3)B、D;(4)2MnO4-+5NO2-+6H+=2Mn2++3H2O+5NO3-;(5)75%;(6)C。
【解析】
试题分析:(1)在装置A烧瓶中浓硝酸与C在加热时发生氧化还原反应,化学方程式为C+4HNO3(浓)  CO2↑+4NO2↑+2H2O;(2)NO2溶于水,与水发生反应产生NO, 3NO2+ H2O == 2HNO3+ NO,产生的硝酸再与Cu发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O。所以 B装置的作用是将NO2转化为NO,同时铜与稀硝酸反应生成NO;(3) CO2是酸性氧化物,可以与碱性发生反应,可以除去NO中的CO2气体的试剂是碱石灰、生石灰,故选项是B、D;(4)亚硝酸盐有还原性,高锰酸钾有强的氧化性,二者会发生反应,离子方程式为2MnO4-+5NO2-+6H+=2Mn2++3H2O+5NO3-;(5)在氧化还原反应中电子转移数目相等,所以5n(MnO4-)=2n(NO2-)+n((NH4)2Fe(SO4)2)。所以在10.00mL的待测溶液中含有的NO2-的物质的量是: n(NO2-)=[5n(MnO4-)- n((NH4)2Fe(SO4)2)]÷2=[(5×0.024L ×0.05mol/L)+×0.01L×0.1 mol/L] ÷2=0.0025mol。所以样品中NaNO2的纯度为[(0.0025mol×69g/mol)÷(2.3g÷10)] ×100%=75%;(6) A.滴定至溶液紫色刚好褪去就立刻停止滴加,则V((NH4)2Fe(SO4)2)体积偏小,会使NaNO2的含量增大,错误;B.加入A与KMnO4溶液前锥形瓶未经干燥,对测定结果不产生任何影响,错误;C.实验中使用的(NH4)2 Fe(SO4)2溶液暴露在空气中时间过长,会被空气中的氧气氧化为Fe3+,则消耗的(NH4)2 Fe(SO4)2溶液的体积偏大,则会使NaNO2的含量偏小,错误。
CO2↑+4NO2↑+2H2O;(2)NO2溶于水,与水发生反应产生NO, 3NO2+ H2O == 2HNO3+ NO,产生的硝酸再与Cu发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O。所以 B装置的作用是将NO2转化为NO,同时铜与稀硝酸反应生成NO;(3) CO2是酸性氧化物,可以与碱性发生反应,可以除去NO中的CO2气体的试剂是碱石灰、生石灰,故选项是B、D;(4)亚硝酸盐有还原性,高锰酸钾有强的氧化性,二者会发生反应,离子方程式为2MnO4-+5NO2-+6H+=2Mn2++3H2O+5NO3-;(5)在氧化还原反应中电子转移数目相等,所以5n(MnO4-)=2n(NO2-)+n((NH4)2Fe(SO4)2)。所以在10.00mL的待测溶液中含有的NO2-的物质的量是: n(NO2-)=[5n(MnO4-)- n((NH4)2Fe(SO4)2)]÷2=[(5×0.024L ×0.05mol/L)+×0.01L×0.1 mol/L] ÷2=0.0025mol。所以样品中NaNO2的纯度为[(0.0025mol×69g/mol)÷(2.3g÷10)] ×100%=75%;(6) A.滴定至溶液紫色刚好褪去就立刻停止滴加,则V((NH4)2Fe(SO4)2)体积偏小,会使NaNO2的含量增大,错误;B.加入A与KMnO4溶液前锥形瓶未经干燥,对测定结果不产生任何影响,错误;C.实验中使用的(NH4)2 Fe(SO4)2溶液暴露在空气中时间过长,会被空气中的氧气氧化为Fe3+,则消耗的(NH4)2 Fe(SO4)2溶液的体积偏大,则会使NaNO2的含量偏小,错误。
考点:考查氧化还原反应方程式的书写、物质的作用、氧化还原反应中物质纯度的计算的知识。

 。
。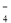 + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O