题目内容
下列表示的轨道正确的是( )
| A、1p | B、2d | C、3f | D、4d |
考点:原子核外电子的能级分布
专题:原子组成与结构专题
分析:根据第1层只有s轨道,第2层有s、p轨道,第3层有s、p、d轨道,第4层有s、p、d、f轨道分析;
解答:
解:由于第1层只有s轨道即1s,第2层有s、p轨道即2s、2p,第3层有s、p、d轨道即3s、3p、3d,第4层有s、p、d、f轨道即4s、4p、4d、4f;所以正确只有D;
故选:D.
故选:D.
点评:本题主要考查了能层与能级的关系,难度不大,注意知识的运用.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
下列说法中正确的是( )
| A、1mol任何物质都含有6.02×1023个原子 |
| B、阿伏加德罗常数就是1mol粒子数的集体,0.012kg12C中含有约6.02×1023个12C |
| C、摩尔是一个基本的物理量 |
| D、1mol水中含有2mol氢和1mol氧 |
某碱性溶液中只有NH4+、Cl-、H+、OH-四种离子.则下列描述正确的是( )
| A、该溶液可由等物质的量浓度、等体积的氨水溶液和盐酸溶液混合而成 |
| B、该溶液可由pH=2的HCl与pH=12的氨水等体积混合而成 |
| C、加入适量的盐酸,溶液中离子浓度为c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、加入适量CH3COOH溶液,c(NH4+)一定大于c(Cl-)、c(CH3COO-)之和 |
下列说法正确的是( )
①分子中都存在共价键;
②质子数相等,电子数也相等的两种微粒可能是不同的离子;
③CO2和SiO2的化学键和晶体类型均相同;
④化学键都有方向性和饱和性;
⑤离子化合物可能含有共价键,共价化合物不含离子键;
⑥固态不导电,熔融状态下能导电的晶体可能为离子晶体.
①分子中都存在共价键;
②质子数相等,电子数也相等的两种微粒可能是不同的离子;
③CO2和SiO2的化学键和晶体类型均相同;
④化学键都有方向性和饱和性;
⑤离子化合物可能含有共价键,共价化合物不含离子键;
⑥固态不导电,熔融状态下能导电的晶体可能为离子晶体.
| A、①④⑤ | B、②③⑥ |
| C、①②④⑤ | D、②⑤⑥ |
(2011?盐城高二质检)下列溶液一定呈中性的是( )
| A、[H+]=[OH-]=10-6 mol?L-1的溶液 |
| B、pH=7的溶液 |
| C、使石蕊试液呈紫色的溶液 |
| D、酸与碱恰好完全反应生成正盐的溶液 |
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德,以下是其中检测出的两种兴奋剂的结构:

关于它们的说法中正确的是( )

关于它们的说法中正确的是( )
| A、Y遇到氯化铁溶液时显紫色,Y能使溴的四氯化碳溶液褪色 |
| B、X含3个手性碳原子 |
| C、1molX与足量氢气反应,最多可消耗5molH2 |
| D、1个Y分子中最多有8个原子共面 |

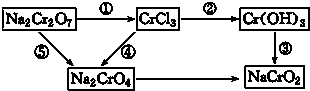 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质.例如:在如图有编号的步骤中,发生氧化反应的是
化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质.例如:在如图有编号的步骤中,发生氧化反应的是 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表: