题目内容
下列表示物质结构的化学用语正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、NaCl的电子式: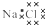 |
C、镁离子的结构示意图: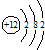 |
D、CH4的比例模型: |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,球棍模型与比例模型
专题:
分析:A.乙烯的官能团为碳碳双键,结构简式中需要标出官能团;
B.氯化钠属于离子化合物,离子化合物的电子式需要标出阴阳离子所带电荷;
C.镁离子的核外电子总数为10,最外层达到8电子稳定结构;
D.甲烷为正四面体结构,根据甲烷的比例模型和球棍模型的表示方法判断.
B.氯化钠属于离子化合物,离子化合物的电子式需要标出阴阳离子所带电荷;
C.镁离子的核外电子总数为10,最外层达到8电子稳定结构;
D.甲烷为正四面体结构,根据甲烷的比例模型和球棍模型的表示方法判断.
解答:
解:A.乙烯分子中含有碳碳双键,乙烯的结构简式为:CH2═CH2,故A错误;
B.NaCl为离子化合物,电子式中需要标出阴阳离子所带电荷,正确的电子式为: ,故B错误;
,故B错误;
C.镁离子的核电荷数为12,核外电子总数为10,最外层为8个电子,镁离子结构示意图为: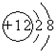 ,故C错误;
,故C错误;
D.比例模型能够体现出各原子相对体积大小及空间结构,甲烷为正四面体结构,碳原子体积大于氢原子,甲烷的比例模型为: ,故D正确;
,故D正确;
故选D.
B.NaCl为离子化合物,电子式中需要标出阴阳离子所带电荷,正确的电子式为:
 ,故B错误;
,故B错误;C.镁离子的核电荷数为12,核外电子总数为10,最外层为8个电子,镁离子结构示意图为:
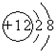 ,故C错误;
,故C错误;D.比例模型能够体现出各原子相对体积大小及空间结构,甲烷为正四面体结构,碳原子体积大于氢原子,甲烷的比例模型为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了常见化学用语的书写判断,题目难度中等,注意掌握电子式、结构简式、比例模型与球棍模型、离子结构示意图与 原子结构示意图的表示方法及区别,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
一定条件下磷与干燥氯气反应,若12.4g磷消耗掉15.68L氯气(标准状况),则产物中PCl3与PCl5的物质的量之比接近于( )
| A、1:2 | B、2:3 |
| C、3:1 | D、5:3 |
已知反应:①Cl2+2KBr═2KCl+Br2,②KClO3+6HCl═3Cl2+KCl+3H2O,③2KBrO3+Cl2═Br2+2KClO3,下列说法正确的是( )
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、氧化性由强到弱顺序为KClO3>KBrO3>Cl2>Br2 |
| C、反应②中还原剂与氧化剂的物质的量之比为5:1 |
| D、③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
下列正确的叙述有( )
①CO2、NO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质.
①CO2、NO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质.
| A、①②③⑤ | B、②③⑤ |
| C、②③ | D、全部 |
下列说法中正确的是( )
| A、H2、2H、H+是三种不同的核素 |
| B、3He和4He互为同位素 |
| C、14C和14N互为同素异形体 |
| D、元素的种类多于核素的种类 |