题目内容
| |||||||||||||||||||||||||||||||||||||||
答案:3.AC;4.BC;
解析:
解析:
(1) |
2Cl--2e- |
(2) |
Ca2++ |
(5) |
蒸发 过滤 |
(6) |
2NaCl+2H2O |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

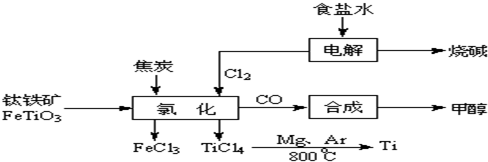
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
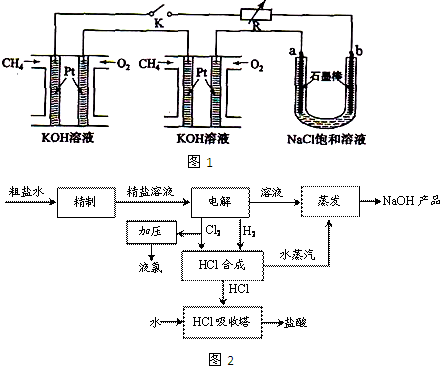




 ____________
____________

 在Ar气氛中进行的理由是________
在Ar气氛中进行的理由是________