题目内容
19.下列描述中,错误的是( )| A. | 往下水道中倾倒硫酸铜溶液,会进一步加快铁制管道的腐蚀 | |
| B. | 镁与稀盐酸反应剧烈,加入醋酸钠晶体可以减慢反应速率 | |
| C. | 电解饱和食盐水制氯气时用铁作阳极 | |
| D. | 电解法精炼粗铜,用纯铜作阴极 |
分析 A.Fe能与硫酸铜发生反应;
B.加入醋酸钠生成醋酸溶液中氢离子浓度减小;
C.金属作阳极失电子;
D.电解法精炼粗铜,用纯铜作阴极,粗铜作阳极.
解答 解:A.Fe能与硫酸铜发生反应生成Cu,Cu、Fe在一起易发生电化学腐蚀,能加快铁制管道的腐蚀,故A正确;
B.镁与稀盐酸反应剧烈,加入醋酸钠生成醋酸溶液中氢离子浓度减小,反应速率减慢,故B正确;
C.金属作阳极失电子,溶液中的阴离子不放电,所以电解饱和食盐水制氯气时用铁作阳极,阳极上不能生成氯气,故C错误;
D.电解法精炼粗铜,用纯铜作阴极,阴极上析出铜单质,粗铜作阳极,粗铜逐渐溶解,故D正确.
故选C.
点评 本题考查较为综合,涉及金属的腐蚀与防护、影响反应速率的因素等知识,侧重于考查学生化学知识的综合运用能量,为考查常见题型,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.糖类、油脂、蛋白质是人体维持生命活动的三大营养物质,下列说法正确的是( )
| A. | 葡萄糖、果糖、蔗糖和淀粉都能发生水解反应 | |
| B. | 利用油脂在碱性条件下的水解,可以制甘油和肥皂 | |
| C. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的高分子化合物 | |
| D. | 淀粉和纤维素的分子组成相同,它们之间互为同分异构体 |
7.下列有关粒子的说法正确的是( )
| A. | 分子一定比原子大 | |
| B. | 所有原子的原子核都是由质子和中子构成 | |
| C. | 分子、原子、离子都是构成物质的粒子 | |
| D. | 物质状态发生变化,是因为粒子大小发生了变化 |
4.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,11.2L 氮气所含的原子数目为NA | |
| B. | 在反应3SiO2+6C+2N2=Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 | |
| C. | 1molNa2O2固体中含离子总数为4 NA | |
| D. | 25℃时pH=13的NaOH溶液中含有Na+的数目为0.1NA |
11.下列说法正确的是( )
| A. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| B. | 铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 | |
| C. | 氢氧燃料电池的能量转换形式之一为化学能转化为电能 | |
| D. | 催化剂通过降低化学反应的焓变加快化学反应速率 |
8.对于某些离子的检验及结论一定正确的是 ( )
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| B. | 加入氢氧化钠溶液,先产生白色沉淀,后迅速变为灰绿色,最后变为红褐色,一定有Fe2+ | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
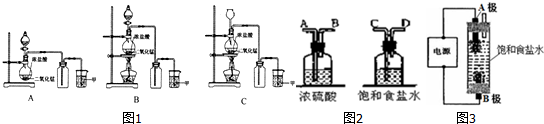
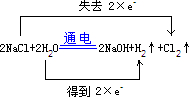 .有人用图3所示装置制取消毒液(主要成分为NaClO),其中A极为阴极,B极为阳极,则阳极的产物为Cl2(填化学式).
.有人用图3所示装置制取消毒液(主要成分为NaClO),其中A极为阴极,B极为阳极,则阳极的产物为Cl2(填化学式). 化学小组的同学利用如图所示装置进行实验.集气瓶中装有纯净物A,分液漏斗中盛有物质B.
化学小组的同学利用如图所示装置进行实验.集气瓶中装有纯净物A,分液漏斗中盛有物质B.
 ),M的一种合成路线如图(部分反应试剂和条件省略).
),M的一种合成路线如图(部分反应试剂和条件省略).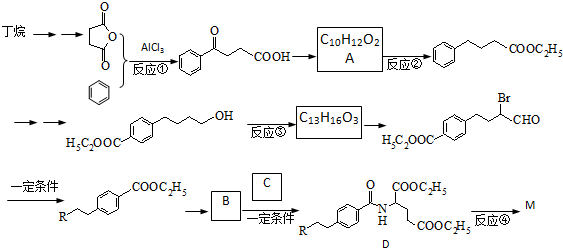
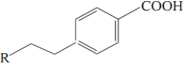 ,C
,C ;
;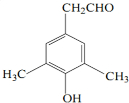 或
或