题目内容
12.化学变化中必然伴随着能量的变化.相同物质的量的氢原子与下列原子结合时放出能量最大的是( )| A. | F | B. | Cl | C. | O | D. | Na |
分析 F、Cl、O、Na原子结构分析可知F的活泼性最大,物质能量越高越活泼,氢原子和选项中原子形成化学键放出能量据此分析,也可以查阅键能大小比较.
解答 解:F、Cl、O、Na原子结构分析可知F的活泼性最大,主要看该物质的氧化性,F氧化性最强具有的能量最高,结合氢原子放出能量最大,查阅数据:HF的键能为565,HCl的键能为431,HO的键能为464,NaH的键能为186,所以最大是A,
故选A.
点评 本题考查了形成化学键能量的变化分析判断,元素原子的活泼些和周期表中存在的递变规律是解题关键,题目较简单.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LCCl4含有NA个分子 | |
| B. | 0.2 mol•L-1 Na2S溶液中含有的S2-数目小于0.2NA | |
| C. | 18gD2O中含有的质子数为10NA(相对原子质量D:2,O:16) | |
| D. | 1molNa与足量的O2反应,钠失去NA个电子 |
3.如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
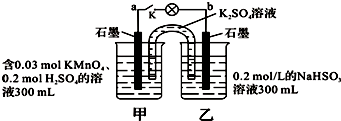

| A. | 当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1 mol•L-1 | |
| B. | 电池工作时,盐桥中的K+移向甲烧杯 | |
| C. | 电池工作时,外电路的电子方向是从a到b | |
| D. | 乙池中的氧化产物为SO42- |
17.a、b、c、d四种元素在周期表中的位置如图,则下列说法正确的是( )


| A. | 若b的最高价氧化物对应水化物为H2bO4,则a的氢化物的化学式为aH3 | |
| B. | 若b的单质可作半导体材料,则c的单质不可能为半导体材料 | |
| C. | 若b的单质与H2易化合,则c的单质与H2更易化合 | |
| D. | a与b之间容易形成离子化合物 |
4.分子式为C5H12O的链状有机物,能与金属钠反应且只两个甲基的同分异构体共有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
1.利用下列表格中的器材和试剂能够完成相应实验的是 ( )
| 选项 | 器材和试剂 | 相应实验 |
| A | 洗气瓶,饱和Na2CO3溶液、浓硫酸、含HCl和水蒸气的CO2气体 | 除去CO2中的HCl和水蒸气 |
| B | 分液漏斗、烧杯、蒸馏水、溴和苯的混合物 | 分离溴和苯的混合物 |
| C | 铁架台、试管、带导管的单孔塞、浓硫酸、铜片 | 实验室制取SO2 |
| D | 铁架台、试管、带导管的单孔塞、棉花、酒精灯、氯化铵晶体、熟石灰 | 实验室制取NH3 |
| A. | A | B. | B | C. | C | D. | D |
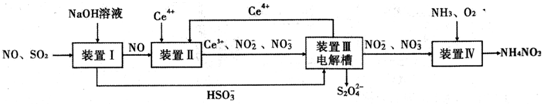
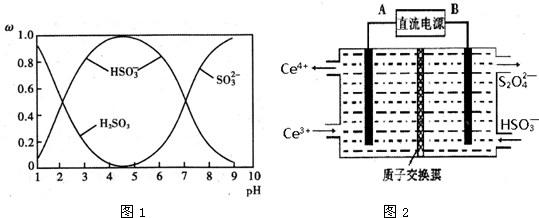
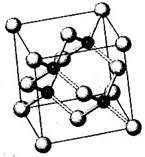 N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题:
N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题: