题目内容
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、2.3gNa在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA |
| B、11.2LCl2所含的原子数为NA |
| C、化学上定义12g碳中的碳原子数为NA的数值 |
| D、1L 0.10mol/L的CuSO4溶液中含Cu2+数目为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、钠完全反应生成钠离子电子转移依据钠的量计算;
B、温度压强不知不能计算物质的量;
C、规定12g12C中所含原子数;
D、n=CV,铜离子水解数目减小.
B、温度压强不知不能计算物质的量;
C、规定12g12C中所含原子数;
D、n=CV,铜离子水解数目减小.
解答:
解:A、钠完全反应生成钠离子电子转移依据钠的量计算,2.3gNa在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA,故A正确;
B、温度压强不知不能计算物质的量,故B错误;
C、规定12g12C中所含原子数为NA的数值,故C错误;
D、n=CV=1L×0.10mol/L=0.1mol,铜离子水解减小,溶液中含Cu2+数目小于0.1NA,故D错误;
故选A.
B、温度压强不知不能计算物质的量,故B错误;
C、规定12g12C中所含原子数为NA的数值,故C错误;
D、n=CV=1L×0.10mol/L=0.1mol,铜离子水解减小,溶液中含Cu2+数目小于0.1NA,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,阿伏伽德罗常数的规定理解,盐类水解的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列说法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、生成物中全部化学键形成时所释放的能量大于破坏反应物中全部化学键所吸收的能量时,反应为吸热反应 |
| D、在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ?mol-1 |
用锌和1mol/L稀硫酸溶液制取氢气,欲提高制取氢气的速率,下列措施不可行的是( )
| A、改用98%的浓硫酸 |
| B、使用更小颗粒的锌粒 |
| C、滴入少量CuSO4溶液 |
| D、加热 |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.8 g乙烯和丙烯的混合物中所含碳原子数为0.2NA |
| B、4.48 L H2和O2的混合物中所含分子数为0.2NA |
| C、4 g重水(D2O)中所含质子数为0.2NA |
| D、200 mL 1 mol/L的氨水中含NH3?H2O分子数为0.2NA |
下列离子方程式中正确的是( )
| A、NaHSO4溶液中加Ba(OH)2溶液至中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3↑+H2O |
| C、高锰酸钾与乙醇制备Mn3O4纳米粉体,同时生成乙醛:6MnO4-+13CH3CH2OH→2Mn3O4+13CH3CHO+6OH-+10H2O |
| D、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
联合制碱法的发明人是中国的科学家( )
| A、华罗庚 | B、钱学森 |
| C、侯德榜 | D、钱三强 |
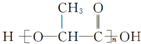 ,有关W的信息如下,其中B能使溴水褪色,C是一个六元状化合物,据此回答下列问题.
,有关W的信息如下,其中B能使溴水褪色,C是一个六元状化合物,据此回答下列问题.