题目内容
能正确表示下列化学反应的离子方程式是( )
| A、向澄清石灰水中通少量二氧化碳:Ca(OH)2+CO2=CaCO3↓+H2O |
| B、稀盐酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、锌片插入硝酸银溶液中:Zn+2Ag+=Zn2++2Ag |
| D、硫酸钠溶液与氯化镁溶液的反应:SO42-+Mg2+=MgSO4↓ |
考点:离子方程式的书写
专题:
分析:A.澄清石灰水与二氧化碳的反应中,氢氧化钙需要拆开,不能保留化学式;
B.铁与稀硫酸反应生成亚铁离子,不会生成铁离子;
C.锌与银离子发生置换反应生成锌离子和银单质;
D.硫酸镁为易溶物,硫酸钠和氯化镁不满足离子反应发生条件,无法写出反应的离子方程式.
B.铁与稀硫酸反应生成亚铁离子,不会生成铁离子;
C.锌与银离子发生置换反应生成锌离子和银单质;
D.硫酸镁为易溶物,硫酸钠和氯化镁不满足离子反应发生条件,无法写出反应的离子方程式.
解答:
解:A.少量二氧化碳与澄清石灰水反应生成碳酸钙、水氢氧化钙应该拆开,正确的离子反应为:Ca2+20H-+C02=H20+CaC03↓,故A错误;
B.铁与稀硫酸反应生成氯化亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.锌片插入硝酸银溶液中,反应生成硝酸锌和银,反应的离子方程式为:Zn+2Ag+=Zn2++2Ag,故C正确;
D.硫酸镁不是难溶物,硫酸钠和氯化镁不发生反应,故D错误;
故选C.
B.铁与稀硫酸反应生成氯化亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.锌片插入硝酸银溶液中,反应生成硝酸锌和银,反应的离子方程式为:Zn+2Ag+=Zn2++2Ag,故C正确;
D.硫酸镁不是难溶物,硫酸钠和氯化镁不发生反应,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
下列关于有机物的说法中,正确的是( )
A、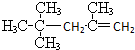 的名称为2,2,4-三甲基戊烯 的名称为2,2,4-三甲基戊烯 |
B、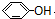 、 、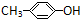 和 和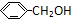 互为同系物 互为同系物 |
| C、CH≡CCH2CH3的所有碳原子在一条直线上 |
D、HCHO和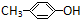 在一定条件下能发生缩聚反应生成 在一定条件下能发生缩聚反应生成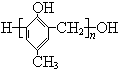 |
几种短周期元素的原子半径及主要化合价如下表:下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | --- | -3 | -2 | |
| A、元素X和Q形成的化合物中不可能含有共价键 |
| B、X、Y、M的单质分别与水反应,Y最剧烈 |
| C、X、Z、R的最高价氧化物的水化物之间可两两相互反应 |
| D、Y的氧化物水化物的酸性一定强于R的氧化物水化物的酸性 |
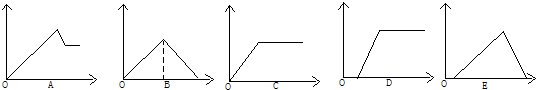
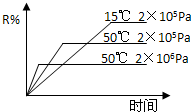 在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X,该反应中R的体积分数如图所示,下列情况正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X,该反应中R的体积分数如图所示,下列情况正确的是( )| A、正反应为吸热反应,X为气体 |
| B、正反应为吸热反应,X为固体或液体 |
| C、正反应为放热反应,X为气体 |
| D、正反应为放热反应,X为固体或液体 |