题目内容
某物质不含碳、氢、氧三种元素,它可能属于的类别是( )
| A、盐类 | B、碱 | C、酸 | D、有机物 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:
分析:根据酸、碱、盐、氧化物的组成特点进行判断;酸的组成特点是它是由氢元素和酸根组成的,碱的组成特点是它是由金属元素和氢氧根组成的,盐的组成特点是它是由金属元素(或铵根)和酸根组成的,氧化物中一定含有氧元素,有机物是一般含碳的化合物.
解答:
解:A、盐由金属元素和酸根构成,可以不含碳、氢、氧元素,例如氯化钠,故A正确;
B、碱是指电离时生成的阴离子全部是氢氧根离子的化合物,所以碱中必含氢元素和氧元素,故B错误;
C、酸是指电离时生成的阳离子全部是氢离子的化合物,所以酸中必含氢元素,故C错误;
D、有机物是含有碳的化合物,故D错误;
故选:A.
B、碱是指电离时生成的阴离子全部是氢氧根离子的化合物,所以碱中必含氢元素和氧元素,故B错误;
C、酸是指电离时生成的阳离子全部是氢离子的化合物,所以酸中必含氢元素,故C错误;
D、有机物是含有碳的化合物,故D错误;
故选:A.
点评:本题考查了物质组成和分类,要想解答好这类题目,要理解和熟记氧化物、酸、碱和盐的概念,以及与之相关的知识.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、0.3mol 氢气中含有氢原子的数目为0.3NA |
| B、标准状况下,4.48L水中含有水分子的数目为0.2NA |
| C、0.2mol?L-1CaCl2溶液中含有氯离子的数目为0.4NA |
| D、2.3g钠与足量水反应,生成钠离子的数目为0.1NA |
下列有关化学方程式或离子方程式书写错误的是( )
| A、将分别蘸有浓盐酸和浓氨水的玻璃棒靠近:NH3+HCl=NH4Cl |
| B、泡沫灭火器的工作原理:3CO32-+2Al3++3H2O=2Al(OH)3↓+3CO2↑ |
| C、在酸性溶液中S2-和SO32-不能共存:2S2-+SO32-+6H+=3S↓+3H2O |
| D、不能用排空气法收集NO气体的原因:2NO+O2=2NO2 |
有关热化学反应描述正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B、CO(g)的燃烧热是283.0kJ/mol,则有下列热化学方程式:2CO2(g)=2CO(g)+O2(g);△H=+566.0kJ/mol |
| C、需要加热才能发生的反应一定是吸热反应 |
| D、1mol甲烷燃烧生成水蒸气和二氧化碳所放出的热量是甲烷的燃烧热 |
水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O
+O2+xOH-═Fe3O4+S4O
+2H2O.下列说法正确的是( )
2- 3 |
2- 6 |
| A、Fe2+、S2O32-都是还原剂 |
| B、每生成1molFe3O4,则转移电子数为3mol |
| C、硫元素被氧化,铁元素被还原 |
| D、x=2 |
下列微粒:①质子 ②中子 ③电子,在所有原子中均含有的微粒是( )
| A、①②③ | B、① | C、①③ | D、①② |
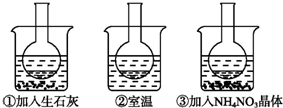 如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.
如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.