��Ŀ����
19����1�����º��������£���ӦFeO��s��+CO��g��?Fe��s��+CO2��g����H��0�ﵽƽ��״̬�ı�־��bc������ĸ����a��������CO2��CO��Ũ��֮��Ϊ1��1 b��v��CO2����=v��CO����
c�����������ܶȱ��ֲ��� d��������ѹǿ���ֲ���
��2��һ���¶��£���2L�ܱ������ڷ�����Ӧ��2SO2��g��+O2��g��?2SO3��g����H=-196kJ•mol-1
�ٵ�����2.8molSO2��1.2molO2������Ӧ���ﵽƽ��ʱ�������ѹǿΪԭ����90%����÷�Ӧ��ƽ�ⳣ��Ϊ0.4�����ٳ���O2��SO3��0.2mol����ʱv����v������д����������=����������
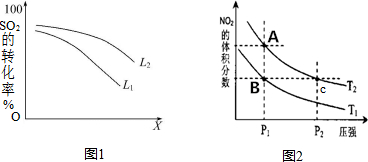
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȣ���ͼ1��ʾLһ��ʱ���÷�SO2ƽ��ת������X�ı仯��ϵ��
X���������������¶ȣ�L1��L2�Ĵ�С��ϵΪL1��L2�����������=����������
��3����֪��ӦN2O4��g��?2NO2��g����H��0���¶ȷֱ�ΪT1��T2ʱ�ﵽ��ƽ��״̬��NO2���������ѹǿ�仯������ͼ2��ʾ��������˵������ȷ����ad��
a��B��C����ķ�Ӧ���ʣ�B��C
b����״̬B��״̬A�������ü��ȵķ���
c��C����ɫ��A����
d��A��C����Ļ�ѧƽ�ⳣ����A��C��
���� ��1����ѧ��Ӧ�ﵽ��ѧƽ��״̬ʱ�����淴Ӧ������ȣ��Ҳ�����0�������ʵ�Ũ�Ȳ��ٷ����仯���ɴ�������һЩ�������������仯���Դ˽����жϣ��ó���ȷ���ۣ�
��2���ٵ�����2.8molSO2��1.2molO2������Ӧ���ﵽƽ��ʱ�������ѹǿΪԭ����90%�������������ʵ�����СΪ��2.8+1.2��mol����1-90%��=0.4mol����
2SO2��g��+O2��g��?2SO3��g�� ���ʵ�����С��n=1
��ʼ����mol����2.8 1.2 0
�仯����mol����0.8 0.4 0.8 0.4
ƽ������mol����2 0.8 0.8
�ٸ���K=$\frac{{c}^{2}��S{O}_{3}��}{{c}^{2}��S{O}_{3}����c��{O}_{2}��}$����ƽ�ⳣ���������ʱŨ����Qc����Qc=K������ƽ��״̬����Qc��K����Ӧ������Ӧ���У���Qc��K����Ӧ���淴Ӧ���У�
������ӦΪ���������С�ķ��ȷ�Ӧ������ѹǿƽ�������ƶ�����������ת�������������¶�ƽ�������ƶ�����������ת���ʼ�С����X�����¶ȣ�L����ѹǿ��
��3��N2O4��g���T2NO2��g����H��0���÷�ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ�������ƶ���NO2�����������������ѹǿ����ѧƽ�������ƶ���NO2�����������С�����ͼ�����������
a��A��C���㶼�ڵ������ϣ�ѹǿԽ��Ӧ����Խ�죻
b��ѹǿ��ͬ�������¶ȣ���ѧƽ�������ƶ���NO2�������������A��NO2�����������
c������ѹǿƽ�����淴Ӧ���У����淴Ӧ�����Ǽ�С����ѹǿ������Ũ���������ƣ�������ƽ���Ա�ԭƽ��Ũ�ȴ�
d��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶���ͬƽ�ⳣ����ͬ��
��� �⣺��1��a��������CO2��CO��Ũ��֮��Ϊ1��1�����Dz����״̬���ʴ���
b��v��CO2����=v��CO����=v��CO��������ƽ��״̬������ȷ��
c�����������ܶȱ��ֲ��䣬˵����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
d�����������������ȣ�������ѹǿʼ�ձ��ֲ��䣬����ȷ����ѡbc��
��2���ٵ�����2.8molSO2��1.2molO2������Ӧ���ﵽƽ��ʱ�������ѹǿΪԭ����90%�������������ʵ�����СΪ��2.8+1.2��mol����1-90%��=0.4mol����
2SO2��g��+O2��g��?2SO3��g�� ���ʵ�����С��n=1
��ʼ����mol����2.8 1.2 0
�仯����mol����0.8 0.4 0.8 0.4
ƽ������mol����2 0.8 0.8
�������Ϊ2L��ƽ�ⳣ��K=$\frac{{c}^{2}��S{O}_{3}��}{{c}^{2}��S{O}_{3}����c��{O}_{2}��}$=$\frac{0��{4}^{2}}{{1}^{2}��0.4}$=0.4��
��ʱŨ����Qc=$\frac{0��{5}^{2}}{1��0.5}$=0.5��K=0.4����Ӧ���淴Ӧ���У���v����v����
�ʴ�Ϊ��0.4������
������ӦΪ���������С�ķ��ȷ�Ӧ������ѹǿƽ�������ƶ�����������ת�������������¶�ƽ�������ƶ�����������ת���ʼ�С����X�����¶ȣ�L����ѹǿ����L2��L1��
�ʴ�Ϊ���¶ȣ�����
��3��a����ͼ���֪��A��C���㶼�ڵ������ϣ�C��ѹǿ����A��C����ķ�Ӧ���ʣ�A��C����a����
b�������¶ȣ���ѧƽ�������ƶ���NO2���������������ͼ���֪��A��NO2�������������T1��T2����״̬B��״̬A�������ü��ȵķ�������b��ȷ��
c����ͼ���֪��A��C���㶼�ڵ������ϣ�C��ѹǿ����A���C��ƽ�����淴Ӧ���У����淴Ӧ���������ڼ�С�������ѹǿ��ƽ���ƶ��Ľ������NO2Ũ���������ƣ�������ƽ���Ա�ԭƽ��Ũ�ȴ�ƽ��ʱNO2Ũ�ȱ�A��Ũ�ȸߣ�NO2Ϊ����ɫ���壬��A��C�����������ɫ��Adz��C���c��ȷ��
d����ͼ���֪��A��C�����������¶Ȳ�ͬ��C�����¶ȸ��ߣ������¶�ƽ��������Ӧ�����ƶ���ƽ�ⳣ�����ʻ�ѧƽ�ⳣ��KA��KC����d����ѡad��
���� ���⿼�黯ѧƽ�ⳣ������Ӧ�á���ѧƽ��ͼ���ؿ���ѧ������������������ͼ��ȡ��Ϣ�������Ѷ��еȣ�

 ����С��ʿ���������ϵ�д�
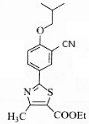
����С��ʿ���������ϵ�д� �������ػ��������ȼ�ϣ���ƫ�����·���ʽ��ͬ�������к�̼̼������ͬ���칹�干�У�������
�������ػ��������ȼ�ϣ���ƫ�����·���ʽ��ͬ�������к�̼̼������ͬ���칹�干�У�������| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
 +
+ $\stackrel{��}{��}$
$\stackrel{��}{��}$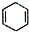 �������й�˵������ȷ���ǣ�������
�������й�˵������ȷ���ǣ�������| A�� | D-A��Ӧ���ڼӳɷ�Ӧ | |
| B�� | 2-��-1��3-����ϩ�ͱ�ϩ����D-A��Ӧ����ֻ��һ�� | |
| C�� | ���Ҫ�ϳ�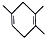 ���õ�ԭʼԭ�Ͽ�����2��3-����-1��3-����ϩ�ͱ�Ȳ ���õ�ԭʼԭ�Ͽ�����2��3-����-1��3-����ϩ�ͱ�Ȳ | |
| D�� | D-A��Ӧ�еIJ��ﶼ����ʹ���Ը��������Һ��ɫ |
| ѡ�� | ʵ������ | ���� |
| A | Cl2��SO2����ʹ���з�̪��NaOH��Һ��ɫ | Cl2��SO2������Ư���� |
| B | Fe��ϡ���ᡢϡ���ᷴӦ�������ݲ��� | Fe��������������û���Ӧ |
| C | ij����ȼ�պ�IJ������ʹ��ɫ����ͭ��ĩ����������ʹ����ʯ��ˮ����� | �����ʿ�����̼�⻯���� |
| D | ��ij�л����ˮ��Һ�м�Na������������ | ���л����п��ܺ����ǻ����Ȼ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��100�桢101��kPa�����£�1��molҺ̬ˮ����ʱ��Ҫ����40.69��kJ����������H2O��g���TH2O��l���ġ�H=+40.69��kJ•mol-1 | |||||||||
| B�� | ��֪CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890.3��kJ•mol-1����CH4��ȼ���ȡ�H=-890.3��kJ | |||||||||
| C�� | H2��g��+Br2��g���T2HBr��g����H=-72��kJ•mol-1����������������
| |||||||||
| D�� | ��֪S��g��+O2��g���TSO2��s����H1��S��g��+O2��g���TSO2��g����H2�����H2����H1 |
| A�� | ���ȷ�Ӧ�ڳ����²�һ���ܹ��Է����� | |
| B�� | �ϳɰ���Ӧ��ʹ�ô�����Ŀ���Ǵٽ��÷�Ӧƽ�������ɰ��ķ����ƶ� | |
| C�� | 0.1 mol•L-1Na2CO3��Һ��35��ʱ���Ա�25��ǿ��˵��Na2CO3ˮ�������ȷ�Ӧ | |
| D�� | MnS����Һ�еμ�����CuSO4��Һ������CuS��������Ksp��CuS����Ksp��MnS�� |
| A�� | �ṹƬ��Ϊ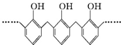 �ĸ߾���䵥���Ǽ�ȩ�ͱ��� �ĸ߾���䵥���Ǽ�ȩ�ͱ��� | |
| B�� | ��ϵͳ���������л��CH3��2CHCH��CH2CH3��CH2CH2CH3����Ϊ��2-��-3-�һ����� | |
| C�� | �ɸʰ��ᡢ�������γɵĶ��������� | |
| D�� | ��ϩ�ͱ�����ʹ��ˮ��ɫ����ɫԭ����ͬ |
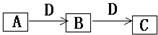 A��B��C��D�����ɶ�����Ԫ����ɵij������ʣ�����A��B��C����ͬһ��Ԫ�أ���һ���������ת����ͼ��ʾ�����ֲ�������ȥ����
A��B��C��D�����ɶ�����Ԫ����ɵij������ʣ�����A��B��C����ͬһ��Ԫ�أ���һ���������ת����ͼ��ʾ�����ֲ�������ȥ����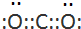 ����A��C��Ӧ�����ӷ���ʽ��OH-+HCO3-=CO32-+H20��
����A��C��Ӧ�����ӷ���ʽ��OH-+HCO3-=CO32-+H20��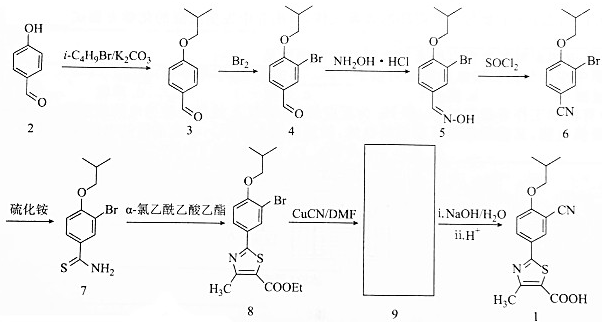
 ��
��