题目内容
5.下列有关热化学方程式的叙述正确的是( )| A. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-53.7kJ/mol,若将含0.1mol醋酸稀溶液与含0.1mol氢氧化钠的稀溶液混合,放出的热量小于5.73kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
分析 A.2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则1mol完全燃烧生成液态水,放出285.8 kJ热量;
B.△H>0,可知反应吸热,石墨能量低;
C.醋酸电离吸热,中和反应为放热反应;
D.物质的量相同的碳,完全燃烧放出的热量大,且焓变为负.
解答 解:A.2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则1mol完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1,故A错误;
B.△H>0,可知反应吸热,石墨能量低,则石墨比金刚石稳定,故B错误;
C.醋酸电离吸热,中和反应为放热反应,由中和热反应可知,生成1molH2O(l)放出热量为57.3kJ,则含0.1mol醋酸稀溶液与含0.1mol氢氧化钠的稀溶液混合,放出的热量小于5.73kJ,故C正确;
D.物质的量相同的碳,完全燃烧放出的热量大,且焓变为负,则△H1<△H2,故D错误;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、燃烧热与中和热为解答的关键,侧重分析与应用能力的考查,注意物质的量与热量成正比,题目难度不大.

练习册系列答案
相关题目
16.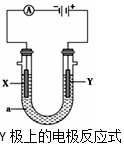 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
 电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:
电解原理在化学工业中有广泛应用.根据如图装置,回答以下问题:(1)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,一段时间后,在X极附近观察到的现象是溶液变蓝、产生气泡,Y极上的电极反应式为4OH--4e-=2H2O+O2↑.
(2)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为1.28g;
(3)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是D (填序号).
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
13.化学与人类生产、生活、社会可持续发展密切相关.下列有关说法不正确的是( )
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| D. | 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水 |
20.在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,3.75mol CuSO4可氧化P的物质的量为( )mol?.生成2mol Cu3P 时,参加反应的P的物质的量为( ) mol?
| A. | 0.75,2.2 | B. | 1.5,2.2 | C. | 0.75,4.4 | D. | 1.5,4.4 |
10.现有三组溶液:①CCl4和水;②苯(沸点:80.1℃)和甲苯(沸点:110.6℃)的混合物(苯和甲苯是性质非常相似的一对互溶液体);③氯化钠和单质碘的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 蒸馏、萃取、分液 | D. | 萃取、蒸馏、分液 |
17.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+、K+、SO4 2-、HCO3 - | B. | Cu2+、K+、SO4 2-、NO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Fe3+、K+、SO4 2-、Cl - |
15.下列说法不正确的是( )
| A. | 氧化还原反应的特征是元素化合价发生了变化 | |
| B. | 在水溶液中能电离出H+的化合物不一定是酸 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定不相同 | |
| D. | 因为NH3溶于水的溶液能导电,所以NH3是电解质 |
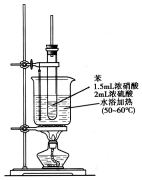 纯硝基苯是一种具有苦杏仁气味的无色油状液体,密度比水大,是制造染料的重要原料,实验室用如图所示的装置来制取.
纯硝基苯是一种具有苦杏仁气味的无色油状液体,密度比水大,是制造染料的重要原料,实验室用如图所示的装置来制取.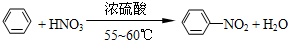 .
.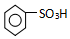 ),导致硝基苯的产率下降.写出发生副反应的化学方程式
),导致硝基苯的产率下降.写出发生副反应的化学方程式 +H2SO4(浓)$\stackrel{△}{→}$
+H2SO4(浓)$\stackrel{△}{→}$