题目内容
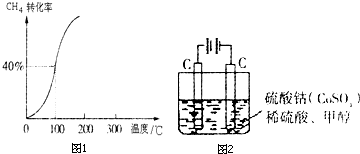
按如图装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述中不正确的是( )


| A、E表示生成铜的物质的量 |
| B、E表示总反应中消耗水的物质的量 |
| C、F表示反应生成氧气的物质的量 |
| D、F表示生成硫酸的物质的量 |
考点:电解原理
专题:
分析:由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,Cu为阴极,发生Cu2++2e-=Cu;由乙可知,转移4mol电子生成2molE,E为Cu,生成1molF,F为氧气,以此来解答.
解答:
解:由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,Cu为阴极,发生Cu2++2e-=Cu,总反应为2CuSO4+2H2O
2Cu+O2↑+2H2SO4,结合乙可知,转移4mol电子生成2molE,生成1molF,
A.由电子与物质的物质的量的关系可知E表示反应生成铜的物质的量,故A正确;
B.由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量,故B正确;
C.由电子与物质的物质的量的关系可知F表示反应生成氧气的物质的量,故C正确;
D.因硫酸与氧气的物质的量不等,则F不能表示生成硫酸的物质的量,故D错误;
故选D.
| ||
A.由电子与物质的物质的量的关系可知E表示反应生成铜的物质的量,故A正确;
B.由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量,故B正确;
C.由电子与物质的物质的量的关系可知F表示反应生成氧气的物质的量,故C正确;
D.因硫酸与氧气的物质的量不等,则F不能表示生成硫酸的物质的量,故D错误;
故选D.
点评:本题考查电解原理,明确发生的电极反应、电解反应及图象的分析是解答本题的关键,注意反应中转移电子与各物质的物质的量的关系即可解答,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、反应热就是反应中放出的能量 |
| B、在任何条件下,化学反应的焓变都等于化学反应的反应热 |
| C、由C(s,石墨)═C(s,金刚石)△H=+1.9kJ?mol-1可知,金刚石比石墨稳定 |
| D、等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
下列物质属于有机物的是( )
| A、CH4 |
| B、Na2CO3 |
| C、CO2 |
| D、CO(NH2)2(尿素) |
1mol气态钠离子和1mol气态氯离子结合生成1mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能.下列热化学方程中,能直接表示出氯化钠晶体格能的是( )
| A、Na+(g)+Cl-(g)═NaCl(s);△H | ||
B、Na(s)+
| ||
| C、Na(s)═Na(g);△H2 | ||
| D、Na(g)-e-═Na+ (g);△H |
已知同温度下溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是( )
| A、Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
| B、Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
| C、Cu2++H2S=CuS↓+2H+ |
| D、FeS+2H+=Fe2++H2S↑ |
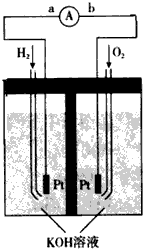 (1)氢氧燃料电池的能量转化主要形式是
(1)氢氧燃料电池的能量转化主要形式是