题目内容
20.向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生反应:2X(g)?Y(g)+3Z(g)(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为0.03mol/(L•min).
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲v(X)=3.5mol/(L•min); 乙v(Y)=2mol/(L•min);
丙v(Z)=4.5mol/(L•min); 丁v(X)=0.075mol/(L•s).
若其它条件相同,温度不同,则温度由高到低的顺序是丁>乙>甲>丙(填序号).
(3)若向达到(1)的平衡体系中充入氩气,则平衡向不移动(填“左“或“右“或“不移动“);若向达到(1)的平衡体系中移走部分混合气体,则平衡向右(填“左“或“右“或“不移动“).
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率 (4)与 (1)的平衡中的X的转化率相比较D.
A.无法确定 B.(4)一定大于 (1)C. (4)一定等于 (1)D. (4)一定小于 (1)
分析 由信息可知:2X(g)?Y(g)+3Z(g)
开始 3mol 0 0
转化 2x x 3x
平衡 3-2x x 3x
反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则$\frac{3-2x+x+3x}{3}$=1.2,解得x=0.3,
(1)Y的物质的量增加0.2mol,结合v=$\frac{△c}{△t}$计算;
(2)依据化学反应速率之比等于化学方程式中计量数之比,把四种情况下的反应速率化为一种物质表示的反应速率减小比较,温度越高反应速率越大;
(3)体积不变平衡体系中充入氩气,平衡体系中各物质的浓度不变;向达到(1)的平衡体系中移走部分混合气体,气体的物质的量减小,相当于减小压强;
(4)若在相同条件下向I的平衡体系中再充入0.5mol X气体,相当于增大压强,平衡逆向进行,X的转化率减小.
解答 解:由信息可知:2X(g)?Y(g)+3Z(g)
开始 3mol 0 0
转化 2x x 3x
平衡3-2x x 3x
反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则$\frac{3-2x+x+3x}{3}$=1.2,解得x=0.3,
(1)Y的物质的量增加0.3mol,由v=$\frac{△c}{△t}$=$\frac{\frac{0.3mol}{2L}}{5min}$=0.03mol/(L.min),故答案为:0.03;
(2)将四个反应速率甲:ν(X)=3.5mol(L•min);乙:ν(Y)=2mol(L•min);丙:ν(Z)=4.5mol(L•min);丁:ν(X)=0.075mol(L•s),都统一到用X表示的反应速率值分别为甲:ν(X)=3.5mol(L•min);乙:ν(X)=4mol(L•min);丙:ν(X)=3mol(L•min);丁:ν(X)=4.5mol(L•min),所以化学反应速率是丁>乙>甲>丙,温度越高,化学反应速率越快,所以温度大小关系是:丁>乙>甲>丙,
故答案为:丁>乙>甲>丙;
(3)体积不变平衡体系中充入氩气,平衡体系中各物质的浓度不变,则平衡不移动;向达到(1)的平衡体系中移走部分混合气体,气体的物质的量减小,相当于减小压强,该反应为气体体积增大的反应,则平衡向右移动,
故答案为:不移动;右;
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,反应体系内的压强增大,平衡向着逆向移动,X的转化率降低,
故答案为:D.
点评 本题考查化学平衡的计算及平衡移动,把握达到平衡后压强与物质的量的变化为解答的关键,侧重分析能力、计算能力的考查,注意平衡计算的格式,题目难度中等.

| A. | 使用合适的催化剂可大大提高生产效率 | |
| B. | 由反应需在300℃进行,可知该反应是吸热反应 | |
| C. | 增大原料气中CO2的百分含量,可以提高H2的转化率 | |
| D. | 70MPa的压力,不仅可以增加单位时间内的产出,还可以提高CO2和H2的利用率 |
| A | |||||||
| B | C | D |
(1)基态C原子含有5种能量不同的电子,其简单离子的电子排布式为1s22s22p6.
(2)DA2+离子的中心原子的杂化轨道类型是sp3,其立体构型为V形.
(3)A所在主族元素的氢化物中,沸点最低的是HCl(填化学式);第一电离能比较:B<C (填“>”、“<”、“=”).
(4)E单质的晶体堆积方式为面心立方密堆积,空间利用率为74%;C与D形成的化合物中化学键类型为共价键.
(5)E的氧化物E2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有16个E原子.若该晶体的密度为ρ g/cm3,则晶胞参数a=$\root{3}{\frac{1152}{ρ•{N}_{A}}}$cm (列出表达式即可).
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | HClO | HNO3 |
| 弱电解质 | HF | BaSO4 | CaCO3 | CH3COOH |
| 非电解质 | Cl2 | CS2 | C2H5OH | SO2 |
| A. | A | B. | B | C. | C | D. | D |
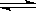 Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答:
Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答: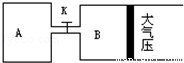
 器恢复原来反应前的体积,可采取的措施是____________________。
器恢复原来反应前的体积,可采取的措施是____________________。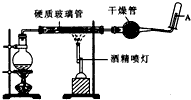 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.