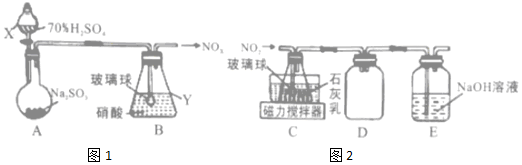
题目内容
9.向3mol•L-1盐酸中加入打磨后的镁条,一段时间后生成灰白色固体X,并测得反应后溶液pH升高.为确认固体X的成分,过滤洗涤后进行实验:①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;
②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;
③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b.
下列分析不正确的是( )
| A. | 溶液pH升高的主要原因:Mg+2H+═Mg2++H2↑ | |
| B. | 生成沉淀a的离子方程式:Ag++Cl-═AgCl↓ | |
| C. | 沉淀b是Mg(OH)2 | |
| D. | 若a、b的物质的量关系为n(a):n(b)=1:3,则可推知固体X的化学式为Mg3(OH)6Cl |
分析 A.据镁条与酸反应,溶液的酸性减弱,pH升高,来分析;
B.据盐酸中氯离子和硝酸银反应来分析;
C.据镁条被盐酸溶解生成镁离子和氢氧根结合生成白色沉淀氢氧化镁来分析;
D.据Ag++Cl-═AgCl↓,Mg2++2OH-═Mg(OH)2↓,进行计算分析.
解答 解:A.据镁条与酸反应即Mg+2H+═Mg2++H2↑,溶液的酸性减弱,pH升高,故A正确;
B.盐酸中氯离子和硝酸银反应,故离子方程式为Ag++Cl-═AgCl↓,故B正确;
C.镁条被盐酸溶解生成镁离子和氢氧根结合生成白色沉淀氢氧化镁,故b是Mg(OH)2,故C正确;
D.设a、b的物质的量分别为1mol,3mol,
Ag++Cl-═AgCl↓
1 1
1 1
则:n(Cl-)=1mol
Mg2++2OH-═Mg(OH)2↓
1 1
3 1
则:n(Mg2+)=3mol,根据电荷守恒得n(OH-)=2n(Mg2+)+n(Cl-)=2×3+1=7mol
故X的化学式为Mg3(OH)7Cl,故D错误;
故选D.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应、白色沉淀的判断为解答的关键,侧重分析与推断能力的考查,注意电荷守恒的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列关于浓硝酸的说法正确的是( )
| A. | 保存在棕色瓶中 | B. | 不易挥发 | C. | 与铜不反应 | D. | 受热不分解 |
20.下列生活中常见用品与其类别或主要成分对应不正确的是( )
| A | B | C | D | |
| 用品名称 |  太阳能电池 |  食用油 |  84消毒液 |  合成纤维宇航服 |
| 类别或 主要成分 | SiO2 | 酯类物质 | 混合物 | 高分子材料 |
| A. | A | B. | B | C. | C | D. | D |
17.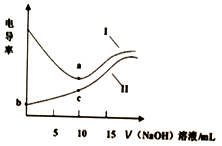 用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )
用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )
 用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )
用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )| A. | b点pH值大于1 | B. | 盐酸浓度为 0.lmol•L-1 | ||
| C. | c点:c(Na+)>c(A-)>c(H+)>c(OH-) | D. | 曲线Ⅰ为盐酸,曲线Ⅱ为醋酸溶液 |
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 100 mL 0.2 mol•L-1蔗糖溶液中所含分子总数为0.02NA | |
| B. | 40mL 10mol•L-1的浓盐酸与足量的MnO2充分反应,生成氯气的分子数为0.1NA | |
| C. | 标准状况下,22.4L CHCl3中含有的氯原子数目为3NA | |
| D. | 14g CO 和N2混合气体中含有的电子总数为7NA |
14.化学与人类生活、生产息息相关,下列说法错误的是( )
| A. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放人生石灰 | |
| B. | 地沟油可以用来制肥皂、提取甘油或者生产生物柴油 | |
| C. | 航天飞船中使用的碳纤维.是一种新型无机非金属材料 | |
| D. | 汽车排放的尾气和冬季取暖排放的顆粒污染物是形成雾霾的一个因素 |
18.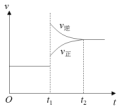 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )| A. | 使用催化剂 | B. | 升高温度 | C. | 增大压强 | D. | 提高 N2浓度 |
11.下列化合物中与自身类别相同的同分异构体数目最多的是( )
| A. | 戊烷 | B. | 丙醇 | C. | 丙酸 | D. | 乙酸乙酯 |