题目内容
7.有A、B、C、D、E、F六种短周期元素,已知A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如右图所示.F的单质可与酸反应,1mol F单质与足量酸反应能产生33.6L H2(标准状况);F的阳离子与A的阴离子核外电子排布完全相同.回答下列问题:| E | A | |||
| B | C | D |
(2)元素D的+1价含氧酸的电子式为
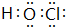 .A在与氢元素形成的化合物中,含有非极性键的化合物的结构式为H-O-O-H.
.A在与氢元素形成的化合物中,含有非极性键的化合物的结构式为H-O-O-H.(3)向D与F形成的化合物的水溶液中加入过量氨水,有关反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
分析 A、B、C、D、E、F六种短周期元素,由位置图可知,E、A在第二周期,B、C、D处于第三周期,设C的质子数为x,则A的质子数为x-8,B的质子数为x-1,D的质子数为x+1,A、B、C、D四种元素原子核外共有56个电子,则x+(x-8)+(x-1)+(x+1)=56,解得x=16,即A为O,B为P,C为S,D为Cl,E为碳,1molF单质与足量酸作用,在标准状况下能产生33.6LH2,设E的化合价为y,根据电子转移守恒:1mol×y=$\frac{3.36L}{22.4L/mol}$×2×1,解得y=3,F的阳离子与A的阴离子核外电子层结构完全相同,则F为Al,然后利用元素及其单质、化合物的性质来解答.
解答 解:A、B、C、D、E、F六种短周期元素,由位置图可知,E、A在第二周期,B、C、D处于第三周期,设C的质子数为x,则A的质子数为x-8,B的质子数为x-1,D的质子数为x+1,A、B、C、D四种元素原子核外共有56个电子,则x+(x-8)+(x-1)+(x+1)=56,解得x=16,即A为O,B为P,C为S,D为Cl,E为碳,1molF单质与足量酸作用,在标准状况下能产生33.6LH2,设E的化合价为y,根据电子转移守恒:1mol×y=$\frac{3.36L}{22.4L/mol}$×2×1,解得y=3,F的阳离子与A的阴离子核外电子层结构完全相同,则F为Al.
(1)C为S元素,在周期表中的位置为:第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)元素D的+1价含氧酸为HClO,电子式为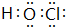 ,A在与氢元素形成的化合物中,含有非极性键的化合物的结构式为H-O-O-H,故答案为:
,A在与氢元素形成的化合物中,含有非极性键的化合物的结构式为H-O-O-H,故答案为: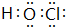 ;H-O-O-H;
;H-O-O-H;
(3)D与F形成的化合物为AlCl3,AlCl3的水溶液中加入过量氨水,反应的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
点评 本题考查元素周期表和元素周期律,元素的推断是解答本题的关键,注意理解同主族元素质子数关系,注意利用电子守恒确定元素化合价.

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案| A. | 大于10.0mL | B. | 小于10.0mL | C. | 等于10.0mL | D. | 等于11.0mL |
| A. | 向Ge(OH)4中加入盐酸:OH-+H+═H2O | |
| B. | MnO2 与浓盐酸反应制Cl2:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O | |
| C. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| D. | 双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O |
| A. | 该电池工作一段时间后,KOH溶液的质量分数不变 | |
| B. | 供电时的总反应为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| C. | 氢氧燃料电池中H2和O2燃烧放出的热量转变为电能 | |
| D. | 该燃料电池可以用两个活性相同的电极 |
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 氯化钙溶液与碳酸钠溶液反应:Ca2++CO32-═CaCO3↓ | |
| C. | 硫酸溶液与碳酸钡反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═H2CO3 |
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | ②③⑤⑦ | B. | ②⑥⑦ | C. | ②④⑤⑥⑦ | D. | ②④⑥ |
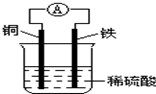
| A. | 铜棒逐渐溶解 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 负极反应式为Fe-2e-=Fe2+,发生还原反应 | |
| D. | 电子由铁棒通过导线流向铜棒 |
| 选项 | A | B | C | D |
| 装 置 图 |  | 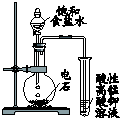 | 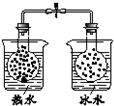 |  |
| 现 象 | 导管中液面上升 | KMnO4溶液褪色 | 热水中的NO2球红棕色加深 | 白色沉淀逐渐转化为黄色沉淀 |
| 结 论 | 该条件下,铁钉发生吸氧腐蚀 | 电石和水反应生成乙炔 | 2NO2(g)?N2O4(g)△H<0 | Ksp:AgCl>AgI |
| A. | A | B. | B | C. | C | D. | D |
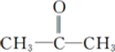 ,
,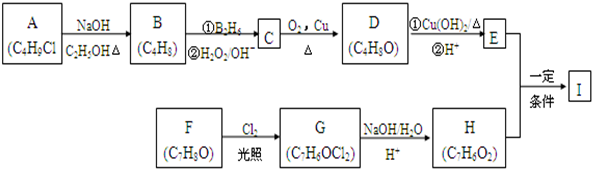
 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
.