题目内容
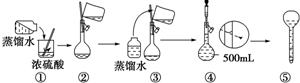
某校课外化学小组设计如下装置制备少量氯气并进行系列实验(夹持及加热仪器已略).
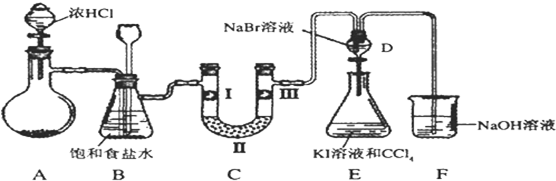
(1)若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置A中的化学反应方程式 ;
(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入一定量氯气时,可以看到D中无色溶液逐渐变为 色,若打开D装置的活塞,使D中溶液滴入E装置,振荡锥形瓶后静置一会儿,可以观察到的现象是 ;
经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明其中不足的原因是 (若不同意,则该空不用写)
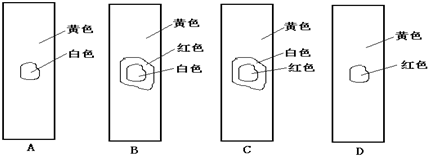
(5)实验后,用玻棒蘸取新制的氯水滴在pH试纸中部,观察到的现象是 (填选项)

(1)若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置A中的化学反应方程式
(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 无水氯化钙 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
经认真考虑,有同学提出该实验方案仍有不足,你若同意该建议,请说明其中不足的原因是
(5)实验后,用玻棒蘸取新制的氯水滴在pH试纸中部,观察到的现象是

考点:氯气的实验室制法,氯气的化学性质
专题:
分析:(1)固体二氧化锰和浓盐酸反应生成氯化锰、氯气和水;
(2)A中制取的氯气含有挥发出来的氯化氢气体,用饱和食盐水可以吸收氯化氢气体;
(3)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(4)当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,可以看到无色溶液逐渐变为橙黄色;说明氯气氧化性强于溴单质;打开活塞,将装置D中少量溶液加入装置E中,生成的溴单质和碘化钾反应生成碘单质,碘单质溶解于四氯化碳中,振荡分层,四氯化碳层在下层;
(5)氯水的成分:含有氯气和次氯酸以及盐酸等成分,具有酸性,次氯酸具有漂白性.
(2)A中制取的氯气含有挥发出来的氯化氢气体,用饱和食盐水可以吸收氯化氢气体;
(3)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(4)当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,可以看到无色溶液逐渐变为橙黄色;说明氯气氧化性强于溴单质;打开活塞,将装置D中少量溶液加入装置E中,生成的溴单质和碘化钾反应生成碘单质,碘单质溶解于四氯化碳中,振荡分层,四氯化碳层在下层;
(5)氯水的成分:含有氯气和次氯酸以及盐酸等成分,具有酸性,次氯酸具有漂白性.
解答:
解:(1)固体二氧化锰和浓盐酸反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)装置B中饱和食盐水的作用是除去氯气中的氯化氢,故答案为:除去Cl2中的HCl;
(3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,选项中abc的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂白性,所以C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,所以选d,故答案为:d;
(4)D中是溴化钠,当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,可以看到无色溶液逐渐变为黄,所以现象为:溶液从无色变化为橙黄色:氧化还原反应中氧化剂的氧化性大于氧化产物,说明氯气的氧化性强于溴;打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,碘单质溶于四氯化碳呈紫红色,振荡.观察到的现象是:E中溶液分为两层,下层(四氯化碳层)为紫红色;
故答案为:橙;E中液体分为两层,下层(CCl4层)为紫红色;
(5)根据氯水的成分:含有氯气和次氯酸以及盐酸等成分,具有酸性,其中次氯酸的漂白是化学漂白,中间的一部分被次氯酸漂白形成白色,而旁边的一部分没有和次氯酸发生反应,所以仍然有指示剂的效用,氯水的酸性使得PH试纸显红色,故选B.
| ||
| ||
(2)装置B中饱和食盐水的作用是除去氯气中的氯化氢,故答案为:除去Cl2中的HCl;
(3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,选项中abc的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂白性,所以C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,所以选d,故答案为:d;
(4)D中是溴化钠,当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,可以看到无色溶液逐渐变为黄,所以现象为:溶液从无色变化为橙黄色:氧化还原反应中氧化剂的氧化性大于氧化产物,说明氯气的氧化性强于溴;打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,碘单质溶于四氯化碳呈紫红色,振荡.观察到的现象是:E中溶液分为两层,下层(四氯化碳层)为紫红色;
故答案为:橙;E中液体分为两层,下层(CCl4层)为紫红色;
(5)根据氯水的成分:含有氯气和次氯酸以及盐酸等成分,具有酸性,其中次氯酸的漂白是化学漂白,中间的一部分被次氯酸漂白形成白色,而旁边的一部分没有和次氯酸发生反应,所以仍然有指示剂的效用,氯水的酸性使得PH试纸显红色,故选B.
点评:本题以氯气的制取及性质检验为载体综合考查实验的相关知识,注意化学方程式的书写、氯水的漂白性,题目难度中等.

练习册系列答案
相关题目
下表中与化学反应相对应的方程式中,正确的是( )
A、化学反应:以石墨作电极电解氯化钠溶液,离子方程式:2Cl-+2H2O
| ||||
| B、化学反应:以银作电极电解硝酸银溶液,离子方程式4Ag++2H2O=4Ag+O2↑+4H+ | ||||
| C、化学反应:铅蓄电池正极反应,离子方程式:PbO2+4H++2e-═Pb2++2H2O | ||||
| D、化学反应:氢氧燃料电池(KOH做电解液)负极反应,离子方程式:O2+4e-+2H2O=4OH- |
金属铝与盐酸反应,下列叙述不正确的是( )
| A、铝作还原剂,氢气做氧化产物 |
| B、该反应属于典型的放热反应 |
| C、如果把该反应设计成原电池,铁、锌均可以做正极 |
| D、标况下,转移2mol 电子,就生成22.4L的氢气 |
Na2CO3俗名纯碱,下列对Na2CO3采用不同分类法的分类.不正确的是( )
| A、Na2CO3是碱 |
| B、Na2CO3是盐 |
| C、Na2CO3是正盐 |
| D、Na2CO3是钠盐 |
部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:下列说法正确的是( )


| A、V=224 |
| B、样品中Fe的质量为2.14g |
| C、样品中CuO的质量为3.52g |
| D、未氧化前Fe元素的质量分数约为41.2% |
如图是某条件时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )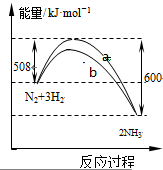

| A、加入催化剂可增大正反应速率,降低逆反应速率 |
| B、正反应的活化能大于逆反应的活化能 |
| C、b曲线是未加入催化剂时的能量变化曲线 |
| D、该反应的热化学方程式为:2NH3?N2+3H2△H=-92 kJ?mol-1 |