题目内容
向一由Fe、Cu组成的混合粉末中加入一定量的稀硝酸,充分反应后剩余金属X g,再各其中加入一定量的稀硫酸,充分振荡后余下金属Y g.则x和y之间的关系是( )
| A、X一定大于Y |
| B、X可能等于Y |
| C、X可能小于Y |
| D、X可能大于Y |
考点:有关混合物反应的计算
专题:计算题
分析:铁与铜的混合物中,加入一定量的稀硝酸,反应后剩余金属Xg,该金属可能为Cu或Cu、Fe;再加入稀硫酸,因硝酸根在酸性条件下具有强氧化性,故剩余金属无论是Cu,还是Cu、Fe混合物,金属都会继续反应,据此进行解答.
解答:
解:在Fe,Cu的混合物中加入一定量的稀硝酸,充分反应后剩余金属X克,该金属可能为Cu或二者的混合物,溶液中一定存在NO3-,加入硫酸后,在酸性条件下NO3-与金属继续反应,则剩余金属进一步溶解,则X一定大于Y,
故选A.
故选A.
点评:本题考查了混合物反应的计算、硝酸的化学性质,题目难度不大,特别注意本题的隐含条件,酸性条件下,硝酸根具有强氧化性,为解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
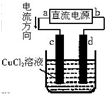 如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )| A、a为负极,b为正极 |
| B、a为阳极,b为阴极 |
| C、电解过程中,c电极质量减少、d电极质量增加 |
| D、如果阴极上有1.6 g铜析出,则阳极上产生气体的体积(标准状况)约为0.56 L |
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| D、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
一种气态烷烃和一种气态烯烃组成的混合物共3.38g,混合气体的密度是相同状况下氢气密度的13倍,让混合气体通过装有溴水的试剂瓶时,试剂瓶的质量增加了2.1g.该混合气体组成可能是( )
| A、CH4和C2H4 |
| B、CH4和C3H6 |
| C、C2H6和C3H6 |
| D、C2H6和C2H4 |
amolH2和bmolC2H2在密闭容器中反应,当其达到平衡时,生成cmol C2H4,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量为( )
A、(
| ||||
| B、(a+3b)mol | ||||
C、(
| ||||
| D、(a+3b+2c)mol |
将Mg、Cu组成的2.64g混合物投入适量的浓硝酸中恰好反应,固体完全溶解使收集到的还原产物NO气体为0.896L(标准状况),向反应后溶液加入2mol/L的NaOH溶液至金属离子恰好完全沉淀.则形成的沉淀质量为( )
| A、4.32 g |
| B、4.68 g |
| C、5.36 g |
| D、6.38 g |
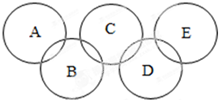 如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空: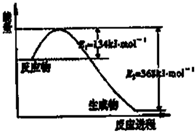 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,