题目内容
 一定温度下,向某容器固定的密闭容器中加入适量(NH4)2S固体,发生如下反应:
一定温度下,向某容器固定的密闭容器中加入适量(NH4)2S固体,发生如下反应:(1)①(NH4)2S(s)?2NH3(g)+H2S(g)
②H2S(g)?H2(g)+S(g)
达到平衡时测得H2S和H2物质的量浓度分别为4mol?L-1和1mol?L-1.则反应①的化学平衡常数K=
(2)25℃时,向20mL0.1mol?L-1 CH3COOH溶液中逐滴加入0.1mol?L-1 NaOH溶液,当NaOH溶液分别加到:①10mL、②20mL、③c(Na+)=c(CH3COO-)、④40mL时,下列说法正确的是
A.①中溶液显酸性,则c(Na+)>c(CH3COOH)
B.②中存在c(CH3COOH)+c(CH3COO-)=0.05mol?L-1
C.③中混合溶液体积大于40mL
D.④中水电离出的c(H+)最大
(3)密闭容器中发生下列反应:A(g)+B(g)?2C(g)△H>0,从起始到t1时刻达到平衡状态,速率变化如图所示.在t2时刻对反应体系升温,t3时刻达到新的平衡,请画出t2-t3的速率变化图(需标出v正、v逆).
(4)已知1.6g液态甲醇在室温时完全燃烧放出的热量为68.4kJ,则该条件下甲醇燃烧的热化学方程式为
(5)室温时,Ksp(CaCO3)=4.96×10-9,Ksp(MgCO3)=6.82×10-6.含有MgCO3沉淀的MgCl2溶液中,已知c(Mg2+)=0.2mol?L-1,如果加入等体积的CaCl2溶液,若要产生CaCO3沉淀,加入CaCl2溶液的物质的量浓度最小约为
考点:化学平衡的计算,热化学方程式,化学电源新型电池,化学反应速率与化学平衡图象的综合应用,难溶电解质的溶解平衡及沉淀转化的本质,酸碱混合时的定性判断及有关ph的计算
专题:化学反应中的能量变化,化学平衡专题,电离平衡与溶液的pH专题
分析:(1)首先根据H2S和H2物质的量浓度分别为4mol?L-1和1mol?L-1计算出平衡时氨气和硫化氢的浓度,然后代入表达式即可;
(2)A.①得等物质量的醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液显酸性;
B.②两者恰好完全反应,得到单一的醋酸钠溶液,体积扩大一倍,根据物料守恒,溶液中存在c(CH3COOH)+c(CH3COO-)=0.05mol?L-1;
C.③c(Na+)=c(CH3COO-)说明溶液呈中性,两者等体积,溶液呈碱性,所以碱少一点,中混合溶液体积小于40mL;
D.④得到等物质量的醋酸钠和氢氧化钠的混合物,以氢氧化钠的电离为主,抵制水的电离,水电离出的c(H+)最小;
(3)密闭容器中发生下列反应:A(g)+B(g)?2C(g)△H>0,从起始到t1时刻达到平衡状态,速率变化如图所示.在t2时刻对反应体系升温,正逆反应速率都增大,升高温度,平衡正向移动,所以v正>v逆;
(4)即0.05mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ,则2mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ×4=2736KJ;负极发生氧化反应;
(5)根据溶度积计算浓度.
(2)A.①得等物质量的醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液显酸性;
B.②两者恰好完全反应,得到单一的醋酸钠溶液,体积扩大一倍,根据物料守恒,溶液中存在c(CH3COOH)+c(CH3COO-)=0.05mol?L-1;
C.③c(Na+)=c(CH3COO-)说明溶液呈中性,两者等体积,溶液呈碱性,所以碱少一点,中混合溶液体积小于40mL;
D.④得到等物质量的醋酸钠和氢氧化钠的混合物,以氢氧化钠的电离为主,抵制水的电离,水电离出的c(H+)最小;
(3)密闭容器中发生下列反应:A(g)+B(g)?2C(g)△H>0,从起始到t1时刻达到平衡状态,速率变化如图所示.在t2时刻对反应体系升温,正逆反应速率都增大,升高温度,平衡正向移动,所以v正>v逆;
(4)即0.05mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ,则2mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ×4=2736KJ;负极发生氧化反应;
(5)根据溶度积计算浓度.
解答:
(1)首先根据H2S和H2物质的量浓度分别为4mol?L-1和1mol?L-1计算出平衡时,氨气和硫化氢的浓度,
平衡时测得H2S和H2物质的量浓度分别为4mol?L-1和1mol?L-1,根据方程式②知参加反应的c(H2S)=1mol/L,①中实际上生成c(H2S)=(4+1)mol/L=5mol/L,根据方程式①得c(NH3)=10mol/L,
所以反应①K=C2(NH3).C(H2S)
=(10mol?L-1)2×4mol?L-1=400,故答案为400;
(2)A.①得等物质量的醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液显酸性,则c(Na+)>c(CH3COOH),故选;
B.②两者恰好完全反应,得到单一的醋酸钠溶液,体积扩大一倍,根据物料守恒,溶液中存在c(CH3COOH)+c(CH3COO-)=0.05mol?L-1,故选;
C.③c(Na+)=c(CH3COO-)说明溶液呈中性,两者等体积,溶液呈碱性,所以碱少一点,中混合溶液体积小于40mL,故不选;
D.④得到等物质量的醋酸钠和氢氧化钠的混合物,以氢氧化钠的电离为主,抵制水的电离,水电离出的c(H+)最小,故不选;
故答案为:AB;
(3)密闭容器中发生下列反应:A(g)+B(g)?2C(g)△H>0,从起始到t1时刻达到平衡状态,速率变化如图所示.在t2时刻对反应体系升温,正逆反应速率都增大,升高温度,平衡正向移动,所以v正>v逆,即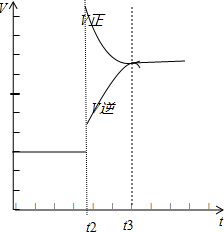 ,故答案为:
,故答案为: ;
;
(4)已知1.6g液态甲醇在室温时完全燃烧放出的热量为68.4kJ,即0.05mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ,则2mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ×4=2736KJ,则该条件下甲醇燃烧的热化学方程式为2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-2736KJ/mol,负极发生氧化反应,所以电极反应式为:CH3OH+H2O-6e-=CO2+6H+,故答案为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-2736KJ/mol,CH3OH+H2O-6e-=CO2+6H+;
(5)要生成沉淀,则应满足c(Ca2+)×c(CO32-)≥4.96×10-9,Ksp(MgCO3)=6.82×10-6,含有MgCO3沉淀的MgCl2溶液中,已知c(Mg2+)=0.2mol?L-1,则混合后MgCl2溶液中c(CO32-)≤3.41×10-5,
则c(CaCl2)=c(Ca2+)=
=
=1.45×10-4mol?L-1,则加入CaCl2溶液的物质的量浓度最小约为1.45×10-4mol?L-1,
故答案为:1.45×10-4mol?L-1.
平衡时测得H2S和H2物质的量浓度分别为4mol?L-1和1mol?L-1,根据方程式②知参加反应的c(H2S)=1mol/L,①中实际上生成c(H2S)=(4+1)mol/L=5mol/L,根据方程式①得c(NH3)=10mol/L,
所以反应①K=C2(NH3).C(H2S)
=(10mol?L-1)2×4mol?L-1=400,故答案为400;
(2)A.①得等物质量的醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液显酸性,则c(Na+)>c(CH3COOH),故选;
B.②两者恰好完全反应,得到单一的醋酸钠溶液,体积扩大一倍,根据物料守恒,溶液中存在c(CH3COOH)+c(CH3COO-)=0.05mol?L-1,故选;
C.③c(Na+)=c(CH3COO-)说明溶液呈中性,两者等体积,溶液呈碱性,所以碱少一点,中混合溶液体积小于40mL,故不选;
D.④得到等物质量的醋酸钠和氢氧化钠的混合物,以氢氧化钠的电离为主,抵制水的电离,水电离出的c(H+)最小,故不选;
故答案为:AB;
(3)密闭容器中发生下列反应:A(g)+B(g)?2C(g)△H>0,从起始到t1时刻达到平衡状态,速率变化如图所示.在t2时刻对反应体系升温,正逆反应速率都增大,升高温度,平衡正向移动,所以v正>v逆,即
 ,故答案为:
,故答案为: ;
;(4)已知1.6g液态甲醇在室温时完全燃烧放出的热量为68.4kJ,即0.05mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ,则2mol液态甲醇在室温时完全燃烧放出的热量为68.4kJ×4=2736KJ,则该条件下甲醇燃烧的热化学方程式为2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-2736KJ/mol,负极发生氧化反应,所以电极反应式为:CH3OH+H2O-6e-=CO2+6H+,故答案为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-2736KJ/mol,CH3OH+H2O-6e-=CO2+6H+;
(5)要生成沉淀,则应满足c(Ca2+)×c(CO32-)≥4.96×10-9,Ksp(MgCO3)=6.82×10-6,含有MgCO3沉淀的MgCl2溶液中,已知c(Mg2+)=0.2mol?L-1,则混合后MgCl2溶液中c(CO32-)≤3.41×10-5,
则c(CaCl2)=c(Ca2+)=
| Ksp(CaCO3) | ||
C(C
|
| 4.96×10-9 |
| 3.41×10-5 |
故答案为:1.45×10-4mol?L-1.
点评:本题考查原电池,明确电池反应中元素的化合价变化发生的反应是解答的关键,化学平衡常数,电解溶液中子浓度大小,溶度积计算浓度,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在Al(OH)3胶体中逐滴加入Ba(OH)2溶液至过量.先出现沉淀,后沉淀溶解 |
| B、SiO2既能和氢氟酸反应又能和氢氧化钠反应,所以它是两性氧化物 |
| C、“冰,水为之,而寒于水”说明相同质量的水和冰,冰的能量更高 |
| D、HCI溶液和NaCl溶液均通过离子导电,所以HCI和NaCl均是离子化合物 |
下列说法中错误的是( )
| A、镁的金属性比钠强 |
| B、溴的非金属性比氯强 |
| C、硝酸的酸性比磷酸强 |
| D、水的热稳定性比氨气强 |
 +
+
 ),则试剂X是
),则试剂X是
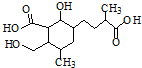 (1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应
(1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应