��Ŀ����
��ѧ����ᡢ���������������أ�����˵����ȷ����
��ʯӢֻ�������������ά���ҳ����²���ǿ�ᷴӦ��
�ڴ���������Һ�����ڻ���������ɱ����
�ۺڻ�ҩ����ơ���ʯ��ľ̿�������ʰ�һ����������Ƴɣ�
����ͭƬ�ڼ��ȵ������¾Ϳɼ���Ũ�����ϡ���
��70mL��H2S��90mL��O2��ϵ�ȼ��ָ���ԭ״���ɲ���70mL��SO2��
������CO2����ͨ��ˮ�����п����ɹ���ʹ���
A���٢ڢܢ� B���٢ڢۢ� C���ڢܢ� D���ڢۢ�
D
��������
�����������ʯӢ������������ᷴӦ�� �ٴ��ڴ���������Һ����ǿ�����ԣ������ڻ���������ɱ��������ȷ���ۺڻ�ҩ����ơ���ʯ��ľ̿�������ʰ�һ����������Ƴɣ�����ȷ����ͭƬ�ڼ��ȵ���������Ũ���ᷴӦ��ϡ�����Ӧ��������ͭƬ�ڼ��������¿ɼ���Ũ�����ϡ���ᣬ����ȷ����70mL��H2S��90mL��O2��ϵ�ȼ��ָ���ԭ״���ɲ���55mL��SO2 ���ݴ�������CO2����ͨ��ˮ�����п����ɹ����С�մ���ѡD��
���㣺STS֪ʶ

������ͼ��ʾ�١�������װ�õ�������ȷ����
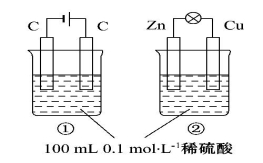
ѡ�� | �� �� | ���� |
A | װ������:�ٵ���,��ԭ��� | ���� |
B | ����Ũ�ȱ仯:������,�ڼ�С | ���� |
C | �缫��Ӧʽ ������:Zn-2e-====Zn2+ :������:4OH--4e-====2H2O+O2�� | ��ȷ |
D | �����ƶ�����:��H+�������ƶ� ��H+�������ƶ� | ��ȷ |
25��ʱ����������ĵ��볣�����£�
����Ļ�ѧʽ | CH3COOH | HCN | H2S |
���볣����25�棩 | 1.8��10-5 | 4.9��10-10 | K1��1.3��10-7 K2��7.1��10-15 |
25��ʱ������˵����ȷ����
A�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH(CH3COONa)> pH(Na2S) > pH(NaCN)
B��a mol/LHCN��Һ��b mol/LNaOH��Һ�������ϣ�������Һ��c(Na+)>c(CN-)����aһ��С�ڻ����b
C��NaHS��Na2S�Ļ����Һ�У�һ������c(Na+)��c(H+)��c(OH-)��c(HS-)��2c(S2-)
D��ijŨ�ȵ�NaCN��Һ��pH��d����������ˮ�������c(OH-)��10-dmol/L
��16�֣�����̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ���⡣
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ�����ڷ���������ϵ����
��C+��KMnO4+��H2SO4 ����CO2��+��MnSO4 +��K2SO4+��
��2������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g) CO2(g)��H2(g)���õ����¶������ݣ�
CO2(g)��H2(g)���õ����¶������ݣ�
ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
��ʵ��1�����£���Ӧ�ӿ�ʼ���ﵽƽ�⣬��v(CO2)��ʾ�ķ�Ӧ����Ϊ ������С������λ������ͬ����
��ʵ��2������ƽ�ⳣ��K= ���÷�ӦΪ ������ȡ����ȡ�����Ӧ��
��3����֪�ڳ��³�ѹ�£�
��2CH3OH(l) +3O2(g)��2CO2(g)+4H2O(g) ��H1 ����1275.6 kJ/mol
��2CO (g)+ O2(g)��2CO2(g) ��H2 ����566.0 kJ/mol
��H2O(g)��H2O(l) ��H3 ����44.0 kJ/mol
д���״�����ȫȼ������һ����̼����̬ˮ���Ȼ�ѧ����ʽ�� ��
��4��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ��ʾ�ĵ��װ�á�

�õ�������ĵ缫��ӦʽΪ ���õ�ع���ʱ����Һ�е�OH���� ����������������ƶ���



 zC(g)��ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A):n(B)�ı仯��ϵ�������н�����ȷ����
zC(g)��ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A):n(B)�ı仯��ϵ�������н�����ȷ����