题目内容
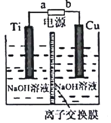
14.用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4-H2C2O4混合溶液.下列叙述错误的是( )| A. | 待加工铝质工件为阳极 | |
| B. | 可选用不锈钢网作为阴极 | |
| C. | 阴极的电极反应式为:Al3++3e-═Al | |
| D. | 硫酸根离子在电解过程中向阳极移动 |
分析 A、铝的阳极氧化法表面处理技术中,金属铝是阳极材料,对应的电极反应为2Al-6e-+3H2O=Al2O3+6H+;
B、阴极材料选择没有特定的要求;
C、阴极上是电解质中的阳离子发生得电子的还原反应;
D、在电解池中,阴离子移向阳极,阳离子移向阴极.
解答 解:A、铝的阳极氧化法表面处理技术中,金属铝是阳极材料,故A正确;
B、阴极不论用什么材料离子都会在此得电子,故可选用不锈钢网作为阴极,故B正确;
C、阴极是阳离子氢离子发生得电子的还原反应,故电极反应方程式为2H++2e-=H2↑,故C错误;
D、在电解池中,阳离子移向阴极,阴离子移向阳极,故硫酸根离子在电解过程中向阳极移动,故D正确,
故选C.
点评 本题主要考查电解原理及其应用.电化学原理是高中化学的核心考点,学生要知道阳极与电池的正极相连发生氧化反应,阴极与电池的负极相连发生还原反应.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
5.下列有关实验原理或操作正确的是( )


| A. | 图1所示的装置可用于干燥、收集并吸收多余的氨气 | |
| B. | 用图2的装置可以验证生铁片在该雨水中是否会发生吸氧腐蚀 | |
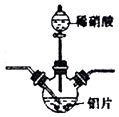
| C. | 图3所示装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| D. | 图4所示装置用于除去碳酸氢钠固体中的少量碳酸钠 |
6.下列关于有机物的叙述正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 分子式为C2H6O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| C. | 油脂和纤维素都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
19. 支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )
支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )
 支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )
支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )| A. | 通入保护电流使钢管桩表面腐蚀电流接近于零 | |
| B. | 通电后外电路电子被强制从高硅铸铁流向钢管桩 | |
| C. | 高硅铸铁的作用是作为损耗阳极材料和传递电流 | |
| D. | 通入的保护电流应该根据环境条件变化进行调整 |
6.根据SO2通入不同溶液中实验现象,所得结论不正确的是( )
| 实验 | 现象 | 结论 | |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
3.以下实验设计能达到实验目的是( )
| 实验目的 | 实验设计 | |
| A. | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
| B. | 制备无水AlCl3 | 蒸发Al与稀盐酸反应后的溶液 |
| C. | 重结晶提纯苯甲酸 | 将粗品水溶、过滤、蒸发、结晶 |
| D. | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
| A. | A | B. | B | C. | C | D. | D |
9.下列物质不属于烃的衍生物的是( )
| A. | CH3CH2Br | B. | 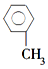 | C. |  | D. | CH3CH2OH |