题目内容
15.在短周期中,X、Y两元素形成的化合物XY2中共有38个电子.若XY2是共价化合物,其化学式是BeCl2、CS2.分析 XY2型化合物,可能为第ⅡA族与ⅤⅡA族元素形成,也可能为第ⅣA族与ⅥA族元素形成,结合共有38个电子、共价化合物条件分析.
解答 解:XY2型化合物,可能为第ⅡA族与ⅤⅡA族元素形成,也可能为第ⅣA族与ⅥA族元素形成,XY2中共有38个电子,3个原子平均每个原子占有电子数大于10,为第二周期和第三周期的元素组成,若为共价化合物,则为非金属元素组成,则为CS2,BeCl2为共价化合物也符合条件,
故答案为:BeCl2、CS2.
点评 本题考查物质的化学式的确定,注意XY2型化合物,可能为第ⅡA族与ⅤⅡA族元素形成,也可能为第ⅣA族与ⅥA族元素形成为解答关键,题目难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
5.下列事实与胶体性质无关的是( )
| A. | 夏日的傍晚常常看到万丈霞光穿云而过,美不胜收 | |
| B. | 食品加工厂利用豆浆中加入盐卤做豆腐 | |
| C. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 某化工厂利用静电除尘技术去除废气中的固体悬浮物 |
6.下列说法正确的是( )
| A. | 在常温常压下,11.2LN2所含有的分子数为0.5NA | |
| B. | 在标准状况下,22.4 L CO和N2的混合物的物质的量为1mol | |
| C. | 在标准状况下,18g H2O的体积为22.4 L | |
| D. | 1mol SO2中原子数为NA个 |
20.将电解质分为强、弱电解质的依据是( )
| A. | 在一定条件下的电离程度 | B. | 属于离子化合物还是共价化合物 | ||
| C. | 熔融状态下是否完全电离 | D. | 溶于水后的导电能力是强还是弱 |
4.下列实验现象不能说明相关结论的是( )
| A. | 将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低 | |
| B. | 将铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性 | |
| C. | 向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动 | |
| D. | 向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物 |
 2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题:
2012年夏,发生在多地的暴雨共造成亿万人受灾.水是组成生命体的重要化学物质,也是一种重要的溶剂,同时也是参与化学反应的重要试剂.怎样利用水为百姓造福将是今后研究的重要课题.请回答下列问题: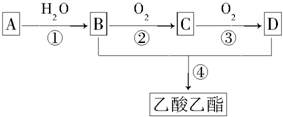
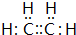 ;C的分子式是C2H4O.
;C的分子式是C2H4O.