题目内容
4.A元素原子的L电子层比B元素原子的L电子层少3个电子,B元素原子核外总电子数比A元素原子电子总数多5个,则A、B形成化合物可能是( )| A. | 离子化合物AB | B. | 离子化合物B2A3 | C. | 离子化合物B(AO3)2 | D. | 离子化合物A2BO3 |
分析 A元素原子的L电子层比B元素的L电子层少3个电子,B元素原子核外总电子数比A元素原子核外总电子数多5个,则A元素原子有2个电子层,B元素原子有3个电子层,故A元素原子L层电子数为8-3=5,故A为氮元素,B元素原子核外总电子数为7+5=12,故B为镁元素.
解答 解:A元素原子的L电子层比B元素的L电子层少3个电子,B元素原子核外总电子数比A元素原子核外总电子数多5个,则A元素原子有2个电子层,B元素原子有3个电子层,故A元素原子L层电子数为8-3=5,故A为氮元素,B元素原子核外总电子数为7+5=12,故B为镁元素,镁元素与氮元素可以形成离子化合物Mg3N2,可以形成离子化合物Mg(NO3)2,
故选:C.
点评 本题考查结构与位置关系等,关键是根据核外电子排布规律推断元素,注意镁与氮气的反应,侧重对基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列物质既可以作防腐剂,又可以作调味剂的是( )
| A. | 味精 | B. | 食盐 | C. | 亚硝酸钠 | D. | 苯甲酸钠 |
15.制出了第一张元素周期表的化学家是( )
| A. | 门捷列夫 | B. | 阿伏伽德罗 | C. | 汤姆生 | D. | 道尔顿 |
12.下列实验相关叙述正确的是( )
| A. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| B. | 实验室常采用铁屑、溴水、苯混合制溴苯 | |
| C. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| D. | 一定物质的量浓度溶液的配置必须要用干燥的容量瓶,否则有误差 |
19.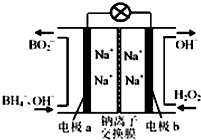 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )| A. | 电池放电时Na+从a极区移向b极区 | |
| B. | 电极a采用MnO2,放电时它被还原 | |
| C. | 该电池负极的电极反应式为:BH4-+8OH--8e-═BO2-+6H2O | |
| D. | 放电时,a极区的电极反应生成碱,碱性增强 |
9.下列关于有机化合物的说法正确的是( )
| A. | 塑料、天然橡胶都是高分子化合物 | |
| B. | 乙烯、聚乙烯和苯分子中均含有碳碳双键 | |
| C. | 棉花、羊毛、蚕丝均属于天然纤维素 | |
| D. | 乙酸和乙醇可用Na2CO3溶液加以区别 |
16.某有机物其结构简式为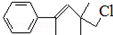 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A. | 分子式为C13H18Cl | |
| B. | 能使酸性KMnO4溶液褪色,但不能使溴水褪色 | |
| C. | 在加热和催化剂作用下,最多能和3mol H2反应 | |
| D. | 该分子中能通过聚合反应生成高分子化合物 |
13.如表实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 将卤代烃加入到热NaOH溶液中一段时间后,取上层液体,加入AgNO3液产生沉淀 | 证明卤代烃中含有卤元素 |
| B | 电石与水反应制得的气体直接通往酸性KMnO4溶液 | 证明制得的气体是否为乙炔 |
| C | 淀粉在硫酸催化作用下水解,将新制氢氧化铜悬浊液加入到水解后的溶液中 | 检验淀粉水解的产物葡萄糖 |
| D | 向纯碱中滴加醋酸,将产生的气体先通入饱和碳酸氢钠溶液再通入苯酚钠浓溶液 | 证明酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
14.下列实验操作中,不能用于物质分离的是( )
| A. | 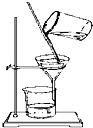 | B. | 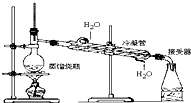 | ||
| C. |  | D. | 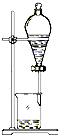 |