题目内容
17.(1)基态Si原子中,电子占据的最高电子层符号为M,该电子层具有的原子轨道数为4,Si原在该层上的电子数为4.(2)Ni2+的价层电子排布图为
 .
.(3)Se原子序数为34,其核外M层电子的排布式为3s23p63d10.
(4)第二周期基态原子未成对电子数与28号元素相同且电负性最小的元素是C.
(5)R基态原子3d轨道的电子数是4s轨道电子数的3倍,其价层电子排布式为3d64s2.
(6)元素Y基态原子的3p轨道上有4个电子,则Y为S.
(7)D元素的正三价离子的3d能级为半充满,D的元素符号为Fe,其原子的结构示意图为
 .
.
分析 (1)硅原子的核外电子排布式为1s22s22p63s23p2,有三层,离原子核越远的电子层其能量越高;该原子第三层即M层中含有1个s轨道、3个p轨道;
(2)镍是28号元素,其原子核外有28个电子,3d、4s电子为其价电子,根据构造原理书写其价电子排布图;
(3)Se是34号,M层已排满;
(4)Ni原子外围电子排布为3d84s2,未成对电子数为2,第二周期基态原子未成对电子数的外围电子排布为2s22p2或2s22p4,同周期自左而右电负性增大,据此分析;
(5)R基态原子3d轨道的电子数是4s轨道电子数的3倍,其价层电子排布式为3d64s2;
(6)Y的核外电子排布式应为1s22s22p63s23p4;
(7)3d半充满则为5个电子,正三价离子是失去最外层4s上的2个电子以及3d上的1个电子.
解答 解:(1)硅原子的核外电子排布式为1s22s22p63s23p2,有三层,离原子核越远的电子层其能量越高;该原子第三层即M层中含有1个s轨道、3个p轨道;M层共有4个电子,故答案为:M;4;4;
(2)Ni核外电子排布为[Ar]3d84s2,则Ni2+价电子排布式是3d8,价电子排布图是 ,故答案为:
,故答案为: ;
;
(3)Se是34号,核外电子排布式为1s22s22p63s23p63d104s24p4,则第三层M层的电子排布式为3s23p63d10,故答案为:3s23p63d10;
(4)Ni原子外围电子排布为3d84s2,未成对电子数为2,第二周期基态原子未成对电子数的外围电子排布为2s22p2或2s22p4,同周期自左而右电负性增大,故未成对电子数与Ni相同且电负性最小的元素是C,故答案为:C;
(5)R基态原子3d轨道的电子数是4s轨道电子数的3倍,其价层电子排布式为3d64s2,故答案为:3d64s2;
(6)Y的核外电子排布式应为1s22s22p63s23p4,16号元素为S,故答案为:S;
(7)3d半充满则为5个电子,正三价离子是失去最外层4s上的2个电子以及3d上的1个电子,则D的核外电子排布式为1s22s22p63s23p63d64s2,是铁元素,原子结构示意图为 ,故答案为:Fe;
,故答案为:Fe; .
.
点评 本题考查核外电子排布,比较基础,根据能量最低原理、洪特规则等书写核外电子排布图,熟悉核外电子排布规律是解题的关键,难度中等.

| A. | Hg、Pb、C、Na | B. | Cu、K、S、P | C. | Hg、Pb、Mn、Ni | D. | Br、N、Pb、As |
| A. | 3:2 | B. | 1:3 | C. | 1:8 | D. | 2:5 |
| A. | 150mL1mol•L-1NaCl溶液 | B. | 100mL2mol•L-1KCl溶液 | ||
| C. | 75mL0.5mol•L-1CaCl2溶液 | D. | 75mL1mol•L-1AlCl3溶液 |
| A. | X-稀盐酸,Y-碳酸钠溶液 | B. | X-偏铝酸钠溶液,Y-硫酸溶液 | ||
| C. | X-硫化氢气体,Y-氯化铁溶液 | D. | X-二氧化碳,Y-偏铝酸钠溶液 |
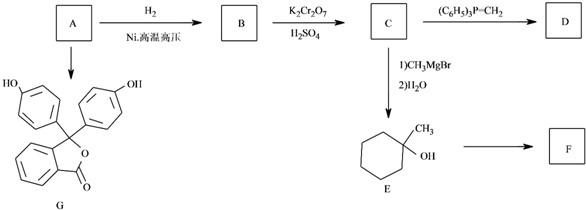
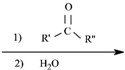
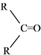 $\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$
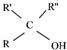
$\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$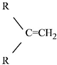 (R表示烃基,R′和R″表示烃基或基)
(R表示烃基,R′和R″表示烃基或基) .
. 、
、 .
. .
.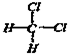 和
和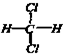
 和
和