题目内容
4.孔雀石的主要成分为Cu2(OH)2CO3,还含少量的FeO、Fe2O3、SiO2.实验室以孔雀石为原料制备CuSO4•5H2O的步骤如图: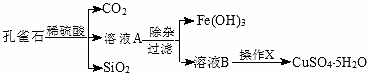
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如表.请回答:
| 物质 | pH (开始沉淀) | pH④ (完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(2)“除杂”时先加入足量H2O2,目的是将Fe2+氧化成Fe3+;再加入CuO固体调节溶液pH的范围至3.2<pH<4.7,其中加入CuO作用是中和溶液中H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀(或调节pH至Fe3+的沉淀范围).
(3)操作X包括蒸发浓缩、冷却结晶、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是抑制Cu2+的水解.
分析 孔雀石的主要成分为Cu2(OH)2CO3,还含少量FeO、Fe2O3、SiO2,加入稀硫酸反应后生成二氧化碳气体,得到溶液A,主要成分为硫酸铜、硫酸亚铁、硫酸铁,过滤得到二氧化硅固体;然后将Fe2+氧化成Fe3+,再加入CuO固体调节溶液pH沉淀铁离子过滤得到滤液为硫酸铜溶液,通过蒸发浓缩,冷却结晶,过滤洗涤得到胆矾晶体,据此解答.
解答 解:孔雀石的主要成分为Cu2(OH)2CO3,还含少量FeO、Fe2O3、SiO2,加入稀硫酸反应后生成二氧化碳气体,得到溶液A,主要成分为硫酸铜、硫酸亚铁、硫酸铁,过滤得到二氧化硅固体;然后将Fe2+氧化成Fe3+,再加入CuO固体调节溶液pH沉淀铁离子过滤得到滤液为硫酸铜溶液,通过蒸发浓缩,冷却结晶,过滤洗涤得到胆矾晶体,
(1)溶液A中的金属阳离子有:Cu2+、Fe2+、Fe3+;由表中数据可知:溶液pH=9.0 时Cu2+也会沉淀;
故答案为:Cu2+、Fe2+、Fe3+;Cu2+也会沉淀;
(2)溶液A中的金属阳离子有:Cu2+、Fe2+、Fe3+,亚铁离子沉淀时铜离子也会沉淀,而铁离子沉淀时铜离子不会沉淀,故应将亚铁离子氧化为铁离子再除去,则需要加氧化剂,双氧水能氧化亚铁离子且不会引入新杂质,由表中数据可知,铁离子沉淀完全的pH为3.2,而铜离子开始沉淀的pH为4.7,调节溶液pH的范围至3.2~4.7之间,CuO固体能中和溶液中H+使溶液的pH升高(1分),促进Fe3+水解生成Fe(OH)3沉淀;
故答案为:将Fe2+氧化成Fe3+; 3.2<pH<4.7 (或3.2~4.7之间);中和溶液中H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀 (或调节pH至Fe3+的沉淀范围);
(3)硫酸铜溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到胆矾晶体,铜离子在水溶液中会水解,应适当酸化抑制其水解;
故答案为:蒸发浓缩;冷却结晶;抑制Cu2+的水解.
点评 本题考查常见金属的单质及其化合物的应用和硫酸铜结晶水含量的测定,掌握物质的制取和提纯、离子的检验等实验操作,分析信息是完成本题目的关键,题目较为综合,难度中等.

①C(s)+H2O(g)═CO(g)+H2(g)△H1=+131.3kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1.
下列有关说法正确的是( )
| A. | 水煤气只能用作燃料 | |
| B. | 水煤气是一种二级能源,比煤直接燃烧污染小 | |
| C. | 等质量的CO和H2完全燃烧时,前者放热多 | |
| D. | 由③反应可以确定H2的燃烧热为241.8 kJ•mol-1 |
| A. | 3.01×1023个双氢青蒿素的质量为142 g•mol-1 | |
| B. | 双氢青蒿素中的C、H、O三种元素的质量比45:6:20 | |
| C. | 7.1 g双氢青蒿素中含有的氢原子总数为1.2NA | |
| D. | 含有NA个碳原子的双氢青蒿素的物质的量为1 mol |
| A. | 12.5% | B. | 14.3% | C. | 48.2% | D. | 87.5% |
| A. | 有丁达尔现象 | B. | 浑浊不透明 | ||
| C. | 能透过滤纸 | D. | 所得分散系不稳定 |
| A. | N4和N2是氮元素的两种不同单质 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互为同位素 | |
| C. | 相同质量的N4和N2所含原子个数比为1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩尔质量是56g/mol |
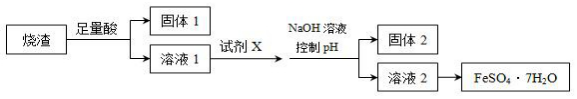
| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH为使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.