题目内容
11.X(g)+3Y(g)?2Z(g)△H=-a kJ•molˉ1,一定条件下,将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol.下列说法正确的是( )| A. | 10min内,Y的平均反应速率为0.03 mol•Lˉ1•sˉ1 | |
| B. | 第10min时,X的反应速率为0.01 mol•Lˉ1•minˉ1 | |
| C. | 10min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10min内,X和Y反应放出的热量为a kJ |
分析 反应10min,测得Y的物质的量为2.4mol,则Y消耗的物质的量为:3mol-2.4mol=0.6mol,根据反应X(g)+3Y(g)?2Z(g)可知,10min内消耗0.2molX、生成0.4molZ;根据v=$\frac{\frac{△n}{V}}{△t}$计算出10min内Y的平均反应速率,然后根据计量数与反应速率成正比得出X的反应速率;该反应为可逆反应,则反应物不可能完全转化成生成物,所以10min内X和Y反应放出的热量小于a kJ,据此进行解答.
解答 解:反应10min,测得Y的物质的量为2.4mol,则Y消耗的物质的量为:3mol-2.4mol=0.6mol,根据反应X(g)+3Y(g)?2Z(g)可知,10min内消耗0.2molX、生成0.4molZ,
A.10min内,Y的平均反应速率为:$\frac{\frac{0.6mol}{2L}}{10min}$=0.03 mol•L-1•min-1,故A错误;
B.化学反应速率与化学计量数成正比,则10min内X的反应速率为:v(X)=$\frac{1}{3}$×v(Y)=0.01mol•L-1•min-1,该速率为平均速率,无法计算及时速率,故B错误;
C.根据分析可知,10min内,消耗0.2molX,生成0.4molZ,故C正确;
D.由于该反应为可逆反应,则1mol X和3molY通入2L的恒容密闭容器中生成Z的物质的量小于2mol,放出的热量小于akJ,故D错误;
故选C.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学反应速率的概念及表达式为解答关键,注意掌握化学平衡及其影响,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
1. 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
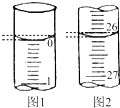
(1)滴定时一般左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶,直到加入最后一滴盐酸,溶液溶液颜色由红色变为无色,且半分钟内不变色,即达到滴定终点.若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸的体积为26.10 mL.
(2)某学生重复三次实验,记录数据如下表所示(待测NaOH溶液的体积均为25.00mL);
计算所测氢氧化钠溶液的物质的量浓度为0.1044 mol/L(保留四位小数)
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏高的是AC.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴处在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定开始时仰视读数,滴定结束时俯视读数.
 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:(1)滴定时一般左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶,直到加入最后一滴盐酸,溶液溶液颜色由红色变为无色,且半分钟内不变色,即达到滴定终点.若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸的体积为26.10 mL.
(2)某学生重复三次实验,记录数据如下表所示(待测NaOH溶液的体积均为25.00mL);
| 滴定次数 | 0.1000mol-L-1盐酸的体积/mL | ||
| 滴定前 | 滴定后 | 体积/mL | |
| 1 | 0.10 | 26.21 | 26.11 |
| 2 | 1.56 | 31.30 | 29.74 |
| 3 | 0.22 | 26.31 | 26.09 |
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏高的是AC.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴处在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定开始时仰视读数,滴定结束时俯视读数.
2.下列各选项有机物数目,与分子式为ClC4H7O2且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)( )
| A. | 分子式为C5H10的烯烃 | B. | 分子式为C4H8O2的酯 | ||
| C. | 甲苯(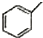 )的一氯代物 )的一氯代物 | D. | 立体烷( 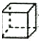 )的二氯代物 )的二氯代物 |
19.下列说法不正确的是( )
| A. | 氯气可用于自来水的消毒 | B. | 镁可用于制造信号弹和焰火 | ||
| C. | 氢氧化铁胶体能用于净水 | D. | 二氧化硫不可用于漂白纸浆 |
6.下列离子方程式正确的是( )
| A. | 二氧化锰和浓盐酸反应:MnO2+4H++4Cl-=Mn2++2Cl2↑+2H2O | |
| B. | 二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O | |
| C. | 碳酸钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 铜和氯化铁溶液反应:Fe3++Cu=Fe2++Cu2+ |
16.向amolNaOH的溶液中通入bmolCO2,下列说法不正确的是( )
| A. | 当a>2b时,发生的离子反应为:2OH-+CO2=CO32-+H2O | |
| B. | 当a<b时,发生的离子反应为:OH-+CO2=HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:3OH-+2CO2=CO32-+HCO3-+H2O | |
| D. | 当0.5a<b<a时,溶液中HCO3-与CO32-的物质的量之比为(a-b):(2b-a) |
20.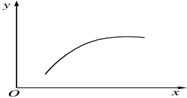 在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g)?2C(g)△H<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g)?2C(g)△H<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合图中曲线的是( )
 在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g)?2C(g)△H<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g)?2C(g)△H<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合图中曲线的是( )| 选项 | x | y |
| A | 温度 | 混合气体的平均相对分子质量 |
| B | 压强 | A的百分含量 |
| C | 再通入A | B的转化率 |
| D | 加入催化剂 | A的质量分数 |
| A. | A | B. | B | C. | C | D. | D |
1.过氧化钙(CaO2)常用作种子及谷物的无毒性消毒剂,常温下为白色的固体,微溶于水,且不溶于乙醇、乙醚或碱性溶液,但溶于酸.某实验小组拟探究CaO2的性质及其实验室制法.
(1)实验探究CaO2与酸的反应.
①CaO2与盐酸反应的化学方程式为2CaO2+4HCl=2CaCl2+2H2O+O2↑.
②加入石蕊后溶液褪色可能是因为溶液a中存在较多的H2O2.
(2)用如图1所示装置制备过氧化钙,其反应原理为Ca+O2$\frac{\underline{\;\;△\;\;}}{\;}$ CaO2
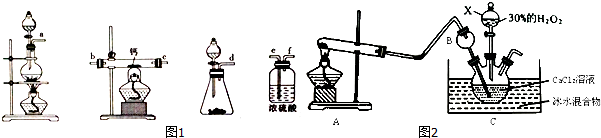
①请选择实验所需的装置,案气流方向连接的顺序为d→e→f→b→c(或d→e→f→c→b)(填仪器接口的字母,上述装置可不选用也可重复使用).
②根据完整的实验装置进行实验,实验步骤如下:Ⅰ.检验装置的气密性后,装入药品;Ⅱ.打开分液漏斗活塞,通入气体一段时间,加热药品;Ⅲ反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞(填操作); IV拆除装置,取出产物.
(3)利用反应Ca2++H2O2+8H2O=CaO2•8H2O↓+2NH4+在碱性环境下制取CaO2的装置如图2所示.
①NH3在Ca2+和 H2O2的反应过程中所起的作用是中和生成的氢离子,促进反应进行.
②反应结束后,经过滤、洗涤、低温烘干可获得CaO2•8H2O,过滤所需要的玻璃仪器是烧杯、漏斗、玻璃棒;将沉淀进行洗涤的操作为沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,让水自然流下,重复2-3次.
(4)设计实验证明CaO2的氧化性比FeCl3的氧化性强:在FeCl2溶液中滴加KSCN溶液,溶液不显红色,再加入少量CaO2粉末,溶液变红色,说明CaO2的氧化性比FeCl3的氧化性强.
(1)实验探究CaO2与酸的反应.
| 操作 | 现象 |
| 向盛有4g CaO2的大试管中加入10mL稀盐酸的溶液a | 剧烈反应,产生能使带火星木条复燃的气体 |
| 取5mL溶液a于试管中,滴入两滴石蕊 | 溶液变红,一段时间后溶液颜色明显变浅,稍后,溶液变为无色 |
②加入石蕊后溶液褪色可能是因为溶液a中存在较多的H2O2.
(2)用如图1所示装置制备过氧化钙,其反应原理为Ca+O2$\frac{\underline{\;\;△\;\;}}{\;}$ CaO2

①请选择实验所需的装置,案气流方向连接的顺序为d→e→f→b→c(或d→e→f→c→b)(填仪器接口的字母,上述装置可不选用也可重复使用).
②根据完整的实验装置进行实验,实验步骤如下:Ⅰ.检验装置的气密性后,装入药品;Ⅱ.打开分液漏斗活塞,通入气体一段时间,加热药品;Ⅲ反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞(填操作); IV拆除装置,取出产物.
(3)利用反应Ca2++H2O2+8H2O=CaO2•8H2O↓+2NH4+在碱性环境下制取CaO2的装置如图2所示.
①NH3在Ca2+和 H2O2的反应过程中所起的作用是中和生成的氢离子,促进反应进行.
②反应结束后,经过滤、洗涤、低温烘干可获得CaO2•8H2O,过滤所需要的玻璃仪器是烧杯、漏斗、玻璃棒;将沉淀进行洗涤的操作为沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,让水自然流下,重复2-3次.
(4)设计实验证明CaO2的氧化性比FeCl3的氧化性强:在FeCl2溶液中滴加KSCN溶液,溶液不显红色,再加入少量CaO2粉末,溶液变红色,说明CaO2的氧化性比FeCl3的氧化性强.
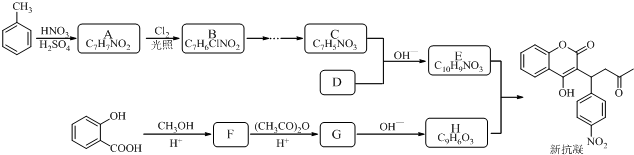
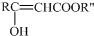
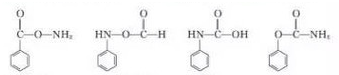
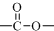 结构;
结构;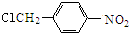 $→_{△}^{NaOH水溶液}$
$→_{△}^{NaOH水溶液}$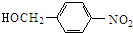 $→_{催化剂}^{O_{2}}$
$→_{催化剂}^{O_{2}}$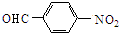
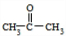 ;E
;E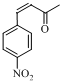
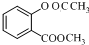 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$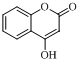 +CH3OH.
+CH3OH.