题目内容
【题目】根据所学知识完成下面题目:
(1)9.5gMgCl2固体溶于水配成500mL溶液,其浓度为molL﹣1 , 从中取出100mL溶液,其中Cl﹣的物质的量为mol;再把取出的溶液加水稀释成500mL,则此时MgCl2溶液的浓度为molL﹣1 .
(2)标准状况下将aLNH3气体溶于1L水中,所得盐酸溶液的密度为bgcm﹣3 , 该溶液物质的量浓度是molL﹣1 .
【答案】
(1)0.2;0.04;0.04
(2)![]()
【解析】解:氯化镁的物质的量= ![]() =0.1mol,溶液物质的量浓度=
=0.1mol,溶液物质的量浓度= ![]() =0.2mol/L;取出100mL溶液,其中Cl﹣的物质的量为0.1L×0.2mol/L×2=0.04mol;溶液是均匀的,从中取出100mL溶液的浓度与原溶液浓度相等,根据稀释定律,稀释后溶液的物质的量浓度=
=0.2mol/L;取出100mL溶液,其中Cl﹣的物质的量为0.1L×0.2mol/L×2=0.04mol;溶液是均匀的,从中取出100mL溶液的浓度与原溶液浓度相等,根据稀释定律,稀释后溶液的物质的量浓度= ![]() =0.04mol/L,所以答案是:0.2;0.04;0.04;(2)标准状况下,aL氨气的物质的量为
=0.04mol/L,所以答案是:0.2;0.04;0.04;(2)标准状况下,aL氨气的物质的量为 ![]() =
= ![]() mol,所以氨气的质量为
mol,所以氨气的质量为 ![]() mol×17g/mol=
mol×17g/mol= ![]() g,所以溶液的质量为1000mL×1g/ml+
g,所以溶液的质量为1000mL×1g/ml+ ![]() g=(1000+
g=(1000+ ![]() )g, 所以溶液的体积为
)g, 所以溶液的体积为 ![]() =
= ![]() L,所以物质的量浓度为
L,所以物质的量浓度为 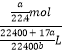 =
= ![]() mol/L,所以答案是:
mol/L,所以答案是: ![]() .
.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目