题目内容
5.下列说法中正确的是( )| A. | NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 | |
| B. | NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 | |
| C. | 在同一能级上运动的电子,其运动状态可能相同 | |
| D. | 若ABn的中心原子A上没有未用于形成共价键的孤对电子,当n=3,则分子结构为三角锥形 |
分析 A、NO2中,N原子的原子核外最外层电子数为5,其在分子中的化合价为+4价,在分子中的原子最外层电子数为9;SO2 分子中S原子最外层电子数为6+4=10,不满足8电子结构;BF3中,B周围只有6e-;
B、NaCl晶胞结构为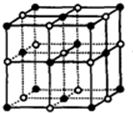 ,晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2;
,晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2;
C、一个电子一种运动状态;
D、若ABn分子的中心原子上没有孤对电子,n=2,则分子的立体构型为直线形,若n=3,则分子的立体构型为平面三角形,若n=4,则分子的立体构型为正四面体形.
解答 解:A、NO2中,N原子的原子核外最外层电子数为5,其在分子中的化合价为+4价,在分子中的原子最外层电子数为9;SO2 分子中S原子最外层电子数为6+4=10,不满足8电子结构;BF3中,B周围只有6e-,所以三种分子各原子的最外层电子数都不满足8e-结构,故A错误;
B、NaCl晶胞结构为 ,NaCl晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2=12,故B正确;
,NaCl晶体中与每个Na+距离相等且最近的Na+个数=3×8÷2=12,故B正确;
C、一个电子一种运动状态,所以同一能级上运动的电子,其运动状态各不同,故C错误;
D、ABn中n=3,无孤电子,则分子结构应为平面三角形,故D错误;
故选B.
点评 本题考查了8e-的稳定,结构分子构型的判断,根据价层电子对互斥理论来分析解答即可,难度不大.

练习册系列答案
相关题目
15.现有葡萄糖、丁醛、乙烯的混合物,若其中氧的质量分数为a,则碳的质量分数是( )
| A. | $\frac{6}{7}$(1-a) | B. | $\frac{3}{4}$a | C. | $\frac{1-a}{7}$ | D. | $\frac{12}{13}$(1-a) |
16.下列有关物质的性质与用途对应关系错误的是( )
| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | NaHCO3受热易分解,可通过加热方法除去碳酸钠中的碳酸氢钠杂质 | |
| C. | Na2O2能与水或二氧化碳反应产生氧气,可用作宇航员的供氧剂 | |
| D. | Al2O3熔点高,可用作耐高温材料 |
13.请选用适当的试剂和分离方法除去下列物质中所含的杂质(括号内为杂质),将所选的试剂及方法的编号填入表中.
试剂:a.水 b.NaOH溶液 c.溴水 d.饱和Na2CO3溶液 e.新制CaO f.饱和NaCl溶液
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 F.盐析
试剂:a.水 b.NaOH溶液 c.溴水 d.饱和Na2CO3溶液 e.新制CaO f.饱和NaCl溶液
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 F.盐析
| 混合物 | 需加入的试剂 | 分离方法 |
| 苯(苯酚) | b | A |
| 乙烷(乙烯) | c | C |
| 乙醇(水) | e | D |
| 乙酸乙酯(乙酸) | d | A |
20.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如表所示:
已知:2min内v(Q)=0.075mol•L-1•min-1,v(Z):v(Y)=1:2.
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(5)该反应达到化学平衡状态时D
A.反应停止了 B.正反应速率与逆反应速率均为0
C.反应物与生成物浓度相等 D.正反应速率与逆反应速率相等.
| 物质 | X | Y | Z | Q |
| 时间 | ||||
| 起始/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(5)该反应达到化学平衡状态时D
A.反应停止了 B.正反应速率与逆反应速率均为0
C.反应物与生成物浓度相等 D.正反应速率与逆反应速率相等.
10.下列有关物质在水溶液中的电离方程式书写正确的是( )
| A. | Na2CO3═2Na++CO32- | B. | AlCl3═Al3++3Cl- | ||
| C. | Mg(NO3)2═Mg+2+2NO3- | D. | KMnO4═K++Mn7++4O2- |
8.下列高分子化合物的认识不正确的是( )
| A. | 有机高分子化合物被称为聚合物或高聚物,是因为它们大部分是由小分子通过聚合反应而得到的 | |
| B. | 有机高分子化合物的相对分子质量很大,因而其结构很复杂 | |
| C. | 对于一块高分子材料来说,n是一个整数值,因而它的相对分子质量是确定的. | |
| D. | 材料可分为天然高分子材料和合成高分子材料两大类 |
9.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是( )
| A. | 通入足量溴水中 | B. | 在空气中燃烧 | ||
| C. | 通入酸性高锰酸钾溶液中 | D. | 通入水中 |