题目内容
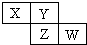 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )| A、X的原子半径大于Y的原子半径 |
| B、W的最高价氧化物对应水化物的酸性比Z的强 |
| C、Y的非金属性比Z的强 |
| D、X与Y形成的化合物都易溶于水 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,由元素在周期表中的位置可知,X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是内层电子数的3倍,则Y原子最外层电子数为6,所以Y为O元素,则X为N元素,Z为S元素,W为Cl元素.
解答:
解:X、Y、Z、W均为短周期元素,由元素在周期表中的位置可知,X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是内层电子数的3倍,则Y原子最外层电子数为6,所以Y为O元素,则X为N元素,Z为S元素,W为Cl元素,
A、同周期元素原子随原子序数递增原子半径而减小,电子层越多原子半径越大,故原子半径X>Y,故A正确;
B、同周期从左到右元素的非金属性增强,则非金属性W>Z,非金属性越强,最高价氧化物对应水化物的酸性越强,所以W的最高价氧化物对应水化物的酸性比Z的强,故B正确;
C、同主族元素从上到下元素的非金属性递减,则非金属性Y>Z,故C正确;
D、X与Y形成的化合物NO不溶于水,故D错误;
故选:D.
A、同周期元素原子随原子序数递增原子半径而减小,电子层越多原子半径越大,故原子半径X>Y,故A正确;
B、同周期从左到右元素的非金属性增强,则非金属性W>Z,非金属性越强,最高价氧化物对应水化物的酸性越强,所以W的最高价氧化物对应水化物的酸性比Z的强,故B正确;
C、同主族元素从上到下元素的非金属性递减,则非金属性Y>Z,故C正确;
D、X与Y形成的化合物NO不溶于水,故D错误;
故选:D.
点评:本题考查位置结构性质关系应用,Y是解答本题的突破口,明确短周期及元素在周期表中的位置来推断,注意基础知识的理解掌握.

练习册系列答案
相关题目
下列说法正确的是( )
| A、酸、碱、盐都是电解质 |
| B、电解质都是易溶于水的物质 |
| C、氧化物都是电解质 |
| D、氢化物都不是电解质 |
某无色溶液中存在大量的NH4+、H+、Clˉ,该溶液中还可能大量存在的离子是( )
| A、CO32ˉ |
| B、OHˉ |
| C、Cu2+ |
| D、Al3+ |
国家环保部对《环境空气质量标准》重新作了修订,向社会征求意见的截止期是2011年12月5日.本次修订的内容有多项,其中有“调整了污染物项目及监测规范”“增设了颗粒物(PM2.5)浓度限值,增设了臭氧8小时平均浓度限值”“调整了污染物项目及监测规范”等等.下列有关说法不正确的是( )
| A、臭氧与空气中的一些碳氢化合物发生作用后会产生光化学烟雾,光化学烟雾对人体健康、植物生长等有严重危害 |
| B、高空中臭氧层能够吸收太阳紫外线,为地球上的生物提供了天然的保护屏障.但低空的臭氧是污染气体,会给人体造成伤害 |
| C、化石类燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产等过程中都是造成二氧化硫污染的重要原因 |
| D、PM2.5是指环境空气中空气动力学当量直径≤2.5μm的颗粒物,也称细颗粒物.直径为2.5μm的颗粒物分散在空气中形成胶体 |
下列说法正确的是( )
| A、宁波从2012年3月25日起公布了空气中的PM2.5,PM2.5是指空气中细颗粒物直径≤2.5u m(1um=10-6m)的颗粒物,它在空气中能形成气溶胶 |
| B、“可燃冰”的燃烧、从海水中得到溴单质、石油分馏全都是化学变化的过程 |
| C、氯化钠、干冰、纯碱属于晶体,具有规则的几何外形和固定的熔点,石蜡、玻璃属于非晶态物质,没有固定的熔点,也不具备规则的几何外形 |
D、原子结构模型的演变历史可表示为: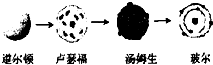 |
氢氧燃料电池已用于航天飞机,它是以铂作电极,以KOH溶液作电解质,下列叙述中不正确的是( )
| A、H2在负极发生氧化反应 |
| B、燃料电池的化学能可以全部转化为电能 |
| C、产物为无污染的水,属于环境友好电池 |
| D、供电时的总反应为:2H2+O2=2H2O |
下列装置所示的实验,能达到实验目的是( )
A、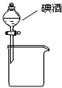 分离碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、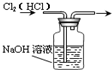 除去Cl2中的HCl |
D、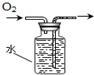 排水集气法收集O2 |
下列电离方程式正确的是( )
| A、Ca(OH)2═Ca2++(OH)2- |
| B、Al2(SO4)3═2Al3++3SO42- |
| C、H2SO4?2H++SO42- |
| D、Na2CO3═Na++CO32- |
葛根素具有降血压等作用,其结构简式如图,下列有关说法正确的是( )
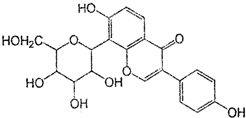

| A、该物质在一定条件下能发生消去反应、加成反应、取代反应 |
| B、葛根素的分子式为C21H22O9 |
| C、该物质一个分子中含有5个手性碳原子 |
| D、一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2 |