题目内容
在常温下 k(CH3COOH)=1.8×10-5。现将0.1mol?L-1的醋酸钠溶液20mL与0.1mol?L-1盐酸10mL在常温下混合后并保持温度不变,下列有关混合溶液中粒子浓度关系正确的是 ( )
A.c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(OH-)
B.c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+)
C.c(CH3COO-)=c(Cl-)=c(CH3COOH)>c(OH-)
D.c(CH3COOH)>c(Cl-)>c(CH3COO-)>c(H+)
A

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案(10分)二甲基亚砜有消炎止痛、镇静等作用。甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3—S—CH3),甲硫醚再与NO2反应制取二甲基亚砜 ( ),有关反应如下:
),有关反应如下:
反应① 2CH3OH(l)+H2S(g)=(CH3)2S(l) +2H2O(l) △H=―akJ·mol-1
反应② (CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g) △H=-bkJ··mol-1
反应③ 2NO(g)+O2(g)=2NO2(g) △H=-ckJ·mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
___________________________________________________, (2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
(2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
| A.v(CH3OH) =" 2v(H2S)" |
| B.恒容容器中,体系的压强不再改变 |
| C.恒容容器中,体系中气体的密度不再改变 |
D.恒容容器中,气体的摩尔质量不 再改变 再改变 |
(4)N2O5是一种新型绿色硝化剂,其制备方法有以下两种。
方法一:4NO2(g)+O2(g) =2N2O5(g)
 ;△H=-56.76 KJ·mol-1
;△H=-56.76 KJ·mol-1 常温下,该反应能逆向自发进行,则逆向反应的△S __________ 0(填“>、<”或“=”)
方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5。工作原理如下图:

硼氢化钠燃料电池的正极反应式________________________。
甲醇是一种可再生能源,具有广泛的开发和应用前景。

(1)工业上一般采用如下反应合成甲醇:
CO(g)+2H2(g) CH2O
H(g)△H= xkJ/mo①右图是反应时CO和CH3 0H的浓度随时间的变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=__ __。
②下表所列数据是该反应在不同温度下的化学平衡
常数(K)
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断x 0(填“<”、“<”填“=”)
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得
c(CO)=0.2mol/L,则CO的转化率为____。
(2)已知在常温常压下
①2CH3OH(1)+3O2(g) 2CO2(g)+4H2O(g) △H=—1275.6kJ/mol
②2CO(g)+O2(g) 2CO2(g)△H=—566.0kJ/mol
③H2O(g) H2O(1)
△H=—44.0kJ/mol
请计算1mol甲醇不完全燃烧生成lmolCO和液态水放出的热量为____。
(3)利用甲醇燃料电池设计如右图所示的装置:
则该装置中b为____极;Cu极的电极反应式为____。
当铜片的质量变化为25.6g时,a极上消耗的O2在标准状况下的体积为_ __L。

 ),有关反应如下:
),有关反应如下:

 二甲基亚砜
二甲基亚砜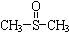 有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜(
有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜(