题目内容
20.对反应:CuSO4+FeS2+H2O→Cu2S+FeSO4+H2SO4,下列说法正确的是( )| A. | FeS2既是氧化剂又是还原剂 | |
| B. | 被氧化的硫和被还原的硫的质量比为3:7 | |
| C. | 氧化剂只有CuSO4 | |
| D. | 1 mol CuSO4可氧化$\frac{5}{7}$mol的硫 |
分析 CuSO4+FeS2+H2O→Cu2S+FeSO4+H2SO4中Cu元素的化合价由+2价降低为+1价,S元素的化合价由-1价降低为-2价,S元素的化合价由-1价升高为+6价,由电子及原子守恒可知配平后的反应为14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,以此来解答.
解答 解:A.S元素的化合价由-1价降低为-2价,S元素的化合价由-1价升高为+6价,则FeS2既是氧化剂又是还原剂,故A正确;
B.由FeS2中S元素的化合价变化及S原子守恒可知,10molS中有3molS失去电子,7molS得到电子,则被氧化的S和被还原的S的质量比为3:7,故B正确;
C.Cu、S元素的化合价降低,则氧化剂为CuSO4、FeS2,故C错误;
D.1 mol CuSO4得到电子为1mol×(2-1)=1mol,由电子守恒可知,可氧化$\frac{1}{7}$mol的S,故D错误;
故选AB.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意S元素的化合价变化为解答的易错点,明确Cu、S元素的化合价变化即可解答,题目难度中等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
10.下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
| A. | 液溴和苯分别受热变为气体 | B. | 干冰和氯化铵分别受热变为气体 | ||
| C. | 二氧化硅和NaCl分别受热熔化 | D. | 食盐和葡萄糖分别溶解在水中 |
11.区别下列各组物质的方法错误的是( )
| A. | 丙烷和丙烯:分别通入酸性KMnO4溶液 | |
| B. | 乙醇和乙酸:分别滴加NaOH溶液 | |
| C. | 苯和四氯化碳:分别加水后静置 | |
| D. | 棉花织品和羊毛织品:分别燃烧闻气味 |
5.下试剂不能一次性鉴别稀HCl、NaCl溶液、Ca(OH)2溶液的是( )
| A. | 紫色石蕊 | B. | 无色酚酞 | C. | pH试纸 | D. | Na2CO3 |
9.常温下,向NH4Cl溶液中通入一定量的NH3,使溶液呈中性,对此溶液说法中,正确的是( )
| A. | c(Cl-)=c(NH4+) | B. | NH4+水解程度增大 | ||
| C. | 氨水电离程度增大 | D. | 溶液中有少量NH4Cl存在 |

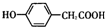 ;写出A与NaHCO3溶液反应的化学方程式
;写出A与NaHCO3溶液反应的化学方程式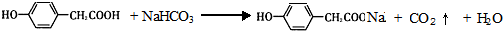 .
.